
【题目】下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。
a | b | ||||||||||||||||
c | d | ||||||||||||||||
e | f | g | h | i | |||||||||||||
j | k | l | m | ||||||||||||||
(1)画出k元素的原子结构示意图______________________________。
(2)写出j元素的原子核外电子排布式___________________________。
(3)写出l元素的+1价阳离子核外电子排布式___________________________。
(4)写出m元素的原子外围电子排布式___________________________,m元素位于周期表中___________周期_________族_________区。
(5)原子半径大小e___________d,第一电离能大小关系是g___________h,电负性大小关系是c___________d(以上填“>”或 “<”)。
【答案】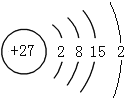 1s22s22p63s23p63d64s2 1s22s22p63s23p63d10 4s24p5 四 VIIA p > < <
1s22s22p63s23p63d64s2 1s22s22p63s23p63d10 4s24p5 四 VIIA p > < <
【解析】
由周期表的相对位置可知,a为H元素、b为He元素、c为N元素、d为O元素、e为Na元素、f为Mg元素、g为Al元素、h为Si元素、i为Cl元素、j 为Fe元素、k为Co元素、l为Cu元素、m为Br元素。
(1)k元素为原子序数为27的Co元素,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)j元素为原子序数为26的Fe元素,原子核外电子排布式为1s22s22p63s23p63d64s2,故答案为:1s22s22p63s23p63d64s2;
(3)l元素为原子序数为29的Cu元素,l元素的+1价阳离子为Cu+,Cu+核外电子排布式为1s22s22p63s23p63d10,故答案为:1s22s22p63s23p63d10;
(4)m元素为原子序数为35的Br元素,Br元素位于元素周期表第四周期VIIA,外围电子排布式为4s24p5,位于元素周期表的p区,故答案为:4s24p5;四;VIIA;p;
(5)同周期元素从左到右,原子半径依次减小,同主族元素从上到下,原子半径依次增大,则钠的原子半径大于氧原子;同周期元素从左到右,第一电离能依次增大,则铝原子第一电离能小于硅;非金属性越强,电负性越大,则氧元素电负性大于氮元素,故答案为:>;<;<。


科目:高中化学 来源: 题型:
【题目】反应2SO2(g)+O2(g) ![]() 2SO3(g)在一容积为2L的密闭容器中进行,试回答:
2SO3(g)在一容积为2L的密闭容器中进行,试回答:
(1)若要加快该反应的反应速率,可采取的措施有____________________、___________________。
(2)开始时,SO2的浓度是2mol/L,O2的浓度是4mol/L,2min内,SO2的浓度减少0.8mol/L,则v(SO2)=_____________。在2min末,SO3的浓度是_______________,O2的浓度是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设C(s)+CO2(g)===2CO(g) ΔH>0,反应速率为v1;N2(g)+3H2(g)===2NH3(g) ΔH<0,反应速率为v2,对于上述反应,当温度升高时,v1和v2的变化情况为( )
A. 同时增大B. 同时减小C. v1增大,v2减D. v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组采用如下方法制作氢氧燃料电池。
(1)如图A所示:a, b均为多孔石墨棒,其中a与直流电源正极相连,b与直流电源负极相连,电解质溶液为NaOH,则图A 中a极称为_______极 (填电极名称)其电极反应式分别为:_____电解总反应化学方程式为 ___________________。(由于使用多孔石墨棒,此时生成的氢气及氧气中有一部分被石墨棒吸附。)
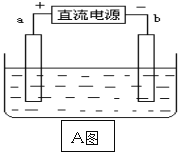
(2)然后如图B所示,移走直流电源,在a, b极间连接一个小灯炮,可以看到灯泡发光。此时的电流方向是 ___________,(填“a→b”或“b→a”)此时a极称为___________(填电极名称)其电极反应式为______________,b极的电极反应式为____________

(3)若图B中氢氧燃料电池改成甲烷燃料电池则b中电极反应式为______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某个容积为2 L的密闭容器内,在T℃时按下图1所示发生反应:
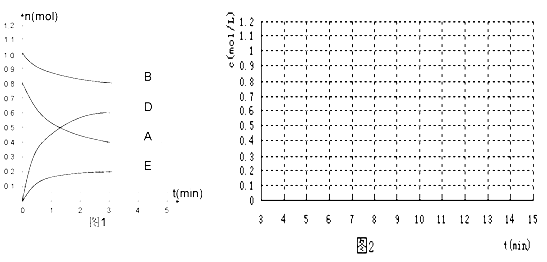
mA(g)+nB(g)![]() pD(g)+qE(s) H<0(m、n、p、q为最简比例的整数)。
pD(g)+qE(s) H<0(m、n、p、q为最简比例的整数)。
(1)根据图1所示,反应开始至达到平衡时,用D表示该反应速率为____________ mol/(L·min);方程式中m:n:p:q =________________
(2)该反应的化学平衡常数K为_________________(保留至一位小数);
(3)下列措施能增大B的转化率的是 ( )
A.升高温度 B.保持体积不变通入1molB
C.保持体积不变移出部分物质D(g) D.将容器的容积增大为原来的2倍
E. 保持体积不变通入1mol A
(4)能判断该反应已经达到化学平衡状态的是( )
A.恒容恒温时容器中气体压强保持不变
B.混合气体中D浓度不变
C.v(A)正 = v(A)逆
D.恒容时容器中气体密度不变
(5)反应达到平衡后,第7 min时,改变条件,在第9min达到新的平衡,在图2上作出第7 min至第15 min(作在答题纸上):下列情况下,D浓度变化图像
①若降低温度且平衡时D物质的量变化了0.4 mol (用虚线)
②若将容器的容积压缩为原来一半(用实线)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
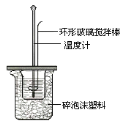
(1)大烧杯上如不盖硬纸板,求得的中和热数值___________(填“偏 大、偏小、无影响”)
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等、不相等”),所求中和热__________(填“相等、不相等”),简述理由__
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会______________;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 4 mol A 气体和 2 mol B 气体在 2 L 的定容容器中混合并在一定条件下发生如下反应 2A(g)+B(g)![]() 2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:
2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:
① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1s-1
② 达到平衡状态时,升高温度,则该化学平衡向左移动,同时化学平衡常数K也减小
③ 2 s 时物质 A 的转化率为70%
④ 达到平衡状态时,增加A物质的量,A和B转化率都提高
⑤当各物质浓度满足c(A)=2c(B)= c(C)时,该反应达到了平衡状态
其中正确的是( )
A. ①③ B. ①② C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MoS2(辉钼矿的主要成分)可用于制取钼的化合物润滑添加剂氢化反应和异构化反应的催化剂等。回答下列问题:
(1)反应3MoS2+18HNO3+12HCl=3H2[MoO2Cl4]+18NO↑+6H2SO4+6H2O中,每溶解1mol MoS2,转移电子的物质的量为___________。
(2)已知:MoS2(s)= Mo(s)+S2(g) △H1
S2(g)+2O2(g)=2SO2(g) △H2
2MoS(s)+7O2(g)=2MoO3 (s)+4SO2(g) △H3
反应2Mo(s)+3O2(g)=2MoO3(s)的△H=___________(用含△H1、△H2、△H3的代数式表示)。
(3)利用电解法可浸取辉钼矿得到Na2MoO4和Na2SO4溶液(装置如图所示)。
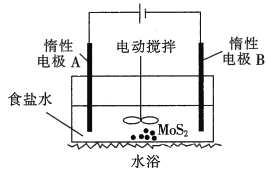
①阴极的电极反应式为______________________。
②一段时间后,电解液的pH___________ (填“增大”“减小”或“不变”),MoO42-在电极___________(填“A”或“B”)附近生成。
③实际生产中,惰性电极A一般不选用石墨,而采用DSA惰性阳极(基层为TiO2,涂层为RuO2+IrO2),理由是_______________________。
(4)用辉钼矿冶炼Mo的反应为
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H。
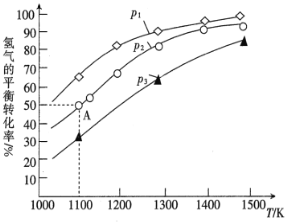
①该反应的△H___________(填“>”或“<”)0;p1、p2、p3按从小到大的顺序为___________。
②在某恒容密闭容器中加入0.1 mol MoS2、0.2mol Na2CO3、0.4mol H2,一定温度下发生上述反应,下列叙述说明反应已达到平衡状态的是____________ (填标号)。
a.v正(H2)=v逆(CO)
b.气体的密度不再随时间变化
c.气体的压强不再随时间变化
d单位时间内断裂H一H键与断裂H—O键的数目相等
③在2L的恒温恒容密闭容器中加入0.1 mol MoS2、0.2 mol Na2CO3、0.4molH2,在1100K时发生反应,达到平衡时恰好处于图中A点,则此温度下该反应的平衡常数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选择适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
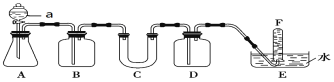
(1)装置A是CO2气体的发生装置,请写出仪器a的名称__________。
(2)B中盛饱和NaHCO3溶液,其作用是___________。
(3)写出C中过氧化钠与二氧化碳反应的化学方程式____________________。
(4)D中盛放的试剂可以是__________(填序号)。
① 浓H2SO4 ② NaOH溶液 ③ CaCl2溶液 ④ Ca(OH)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com