
Q、R、X、Y、Z五种元素的原子序数依次递增.已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子排布为msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4.
请回答下列问题:
(1)Z2+的核外电子排布式是 .
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的 形成配位键.
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 .
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为 (用元素符号作答).
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为 .
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 (填晶体类型).
考点: 原子核外电子排布;元素电离能、电负性的含义及应用;共价键的形成及共价键的主要类型;配合物的成键情况.
专题: 原子组成与结构专题;化学键与晶体结构.
分析: Q、R、X、Y、Z五种元素的原子序数依次递增,①Z的原子序数为29,其余的均为短周期主族元素,则Z是Cu元素;
③R原子核外L层电子数为奇数,且属于短周期主族元素,所以R是第二周期元素,Q的原子序数小于R,则Q属于第一或第二周期元素;
④Q、X原子p轨道的电子数分别为2和4,则Q是C元素,R是N或F元素;
X原子P轨道含有4个电子且原子序数大于R,所以X是O或S元素,
②Y原子价电子排布为msnmpn,原子序数小于29,n=2,Y原子序数大于X,且属于主族元素,所以Y是Si元素,则X是O元素,R是N元素,
则Q、R、X、Y、Z五种元素分别是C、N、O、Si、Cu.
解答: 解:Q、R、X、Y、Z五种元素的原子序数依次递增,①Z的原子序数为29,其余的均为短周期主族元素,则Z是Cu元素;
③R原子核外L层电子数为奇数,且属于短周期主族元素,所以R是第二周期元素,Q的原子序数小于R,则Q属于第一或第二周期元素;
④Q、X原子p轨道的电子数分别为2和4,则Q是C元素,R是N或F元素;
X原子P轨道含有4个电子且原子序数大于R,所以X是O或S元素,②Y原子价电子排布为msnmpn,原子序数小于29,n=2,Y原子序数大于X,且属于主族元素,所以Y是Si元素,则X是O元素,R是N元素,
则Q、R、X、Y、Z五种元素分别是C、N、O、Si、Cu.
(1)Z为Cu元素,Z2+为Cu2+,Cu的价电子排布为3d104s1,失去两个电子,则为3d9,Cu2+的核外电子排布式是1s22s22p63s23p63d9,
故答案为:1s22s22p63s23p63d9;
(2)含有孤电子对的原子和含有空轨道的原子之间能形成配位键,在[Cu(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的孤电子对形成配位键,
故答案为:孤电子对;
(3)Q、Y的氢化物分别为CH4和SiH4,由于C的非金属性强于Si,则稳定性CH4>SiH4.因为SiH4 的相对分子质量比CH4大,故分子间作用力大,沸点高,
故选:b.
(4)C、N和Si中,C、Si位于同一主族,则上面的非金属性强,故第一电离能大,即Si<C,而N由于具有半充满状态,故第一电离能比相邻元素大,C<N,所以第一电离能Si<C<N.
故答案为:Si<C<N;
(5)Q为C元素,C、H形成的相对分子质量为26的物质为C2H2,结构式为H﹣C≡C﹣H,单键是σ键,叁键中有两个是σ键一个π键,所以σ键与π键数之比为3:2,
故答案为:3:2;
(6)电负性最大的非金属元素是O,最小的非金属元素是Si,两者构成SiO2,属于原子晶体,故答案为:原子晶体.
点评: 本题以元素推断为载体,考查物质结构与性质、核外电子排布、电离能、化学键、晶体等,是对所学知识的综合运用,难度中等,根据原子结构推断元素是解题关键,注意基础知识的掌握.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
下列离子方程式中正确的是
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO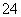 ===BaSO4↓+H2O
===BaSO4↓+H2O
B.向NaOH溶液中滴入少量Ca(HCO3)2溶液:Ca2++HCO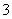 +OH-===CaCO3↓+H2O
+OH-===CaCO3↓+H2O
C.Na2CO3溶液中通入CO2:CO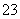 +CO2+H2O===2HCO
+CO2+H2O===2HCO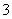
D.CH3COOH溶液与NaOH溶液反应:H++OH-===H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
验证某有机物属于烃,应完成的实验内容的是( )
A.只测定它的C、H原子个数比
B.只要证明它完全燃烧后产物只有H2O和CO2
C.只测定其燃烧产物中H2O和CO2的物质的量之比
D.只测定该试样的质量及试样完全燃烧后生成H2O和CO2的质量
查看答案和解析>>
科目:高中化学 来源: 题型:
将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL 2mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量为( )
A. 0.2mol B. 0.6mol C. 0.8mol D. 1.0mol
查看答案和解析>>
科目:高中化学 来源: 题型:
丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1g·mL-1,沸点约为55℃。要从水与丙酮的混合物中将丙酮分离出来,你认为下列方法中最为合理的是 ( )
A.蒸馏 B.分液 C.过滤 D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
已知14.2g X气体在标准状况下的体积是4.48L,则X气体的摩尔质量是 ( )
A.71g B.71 C.71g /mol D.142g /mol
查看答案和解析>>
科目:高中化学 来源: 题型:
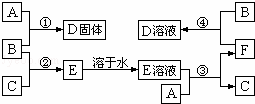
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体.在合适反应条件下,它们可以按下面框图进行反应;又知单质A是当今世界产量最大的金属,E的溶液是无色的.请回答:
(1)A是 ,B是 ,C是 (请填写化学式);
(2)反应①的化学方程式 ;
(3)反应③的离子方程式 ;
(4)反应④的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com