
双氧水可作为采矿业废液的处理剂,如用来消除采矿废液中的氰化物,反应方程式如下:KCN+H2O2+H2O===A+NH3↑。下列说法正确的是
A.生成物A是一种正盐 B.氨气是还原产物
C.该反应中H2O2作氧化剂 D.处理1 mol KCN转移1 mol电子
科目:高中化学 来源: 题型:
某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:

①图中X溶液是_____________________________;
②石墨电极上发生的电极反应式为__________________________________________;
③原电池工作时,盐桥中的____________(填“K+”或“Cl-”)不断进入X溶液中。
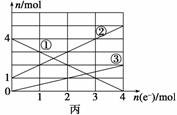
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是__________极;
②图丙中的②线是______________的变化。
③当电子转移为2 mol时,向乙烧杯中加入________ L 5 mol·L-1 NaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O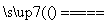 Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________________________________。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________________________________。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将Al片和Cu片用导线相连,插入稀H2SO4溶液中组成原电池,写出电极名称及电极反应式:
Al片( )_______________________________________________________________
(2)若将Al片和Cu片用导线相连,插入浓HNO3中能否组成原电池?________(填“能”或“不能”),若能组成原电池,写出电极名称及电极反应式:
Al片( )__________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是
A.F2、K、HCl B.Cl2、Al、H2
C.SO2、Na、Br2 D.O2、SO2、H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的:①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.②④⑥ B.①② C.②③⑤ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
锅炉水垢既会降低燃料的利用率、影响锅炉的使用寿命,还可能造成安全隐患。
某锅炉水垢的主要成分有CaCO3、CaSO4、Mg(OH)2、Fe2O3,用酸洗法可除去该水垢,其基本原理如下图所示。
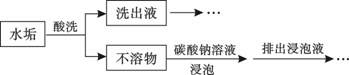
(1)酸洗时,为使水垢尽可能溶解,不宜选用的是 (填标号)。
A.醋酸 B.盐酸 C.硝酸 D.稀硫酸
(2)不溶物用碳酸钠溶液浸泡时,反应的离子方程式是 。
(3)洗出液中的Fe3+会腐蚀铁质管道,反应的离子方程式是 ,因此,常在洗出液中加入具有强还原性的SnCl2溶液,反应中的Sn2+与Fe3+的物质的量之比为1∶2,Sn2+转化为 (填离子符号)。
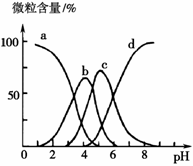
(4)柠檬酸(用H3R表示)可用作酸洗剂,溶液中
H3R、H2R-、HR2-、R3-的含量与pH的关系如图
所示。图中a曲线所代表的微粒的百分含量随溶液
pH的改变而变化的原因是 。
调节柠檬酸溶液的pH=4,有利于除去水垢中的氧化
铁。pH=4时,溶液中上述4种微粒含量最多的
是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
三氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120o,它能水解,有关叙述正确的是( )
A.三氯化硼液态时能导电而固态时不导电 B.硼原子以sp杂化
C.三氯化硼遇水蒸气会产生白雾 D.三氯化硼分子属极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素基态原子的外围电子排布为4d15s2,下列说法正确的是
A.该元素原子最外层共有3个电子 B.该元素原子核外有5个电子层
C.该元素在周期表中属于s区元素 D.该元素原子M层共有8个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com