
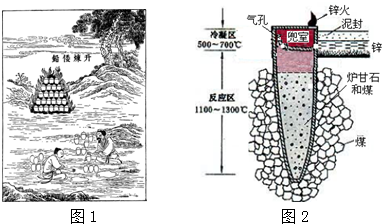
| A. | “泥封”的目的是为了防止得到的锌被氧化 | |
| B. | “锌火”是锌蒸气和一氧化碳在空气的燃烧 | |
| C. | 冶炼时锌变为蒸气在兜室冷凝为固体 | |
| D. | 升炼倭铅过程包含分解反应和氧化还原反应 |
分析 “升炼倭铅”的反应:ZnCO3$\frac{\underline{\;500℃\;}}{\;}$CO2↑+ZnO、CO2+C$\frac{\underline{\;>900℃\;}}{\;}$2CO、ZnO+CO$\frac{\underline{\;>907℃\;}}{\;}$Zn(g)+CO2,
A.Zn易被空气氧化;
B.CO是可燃性气体,易燃烧;
C.反应区温度达到1100~1300℃,Zn变为蒸气与杂质分离,在“兜室”冷凝为液体;
D.由一种物质生成两种或多种物质的反应是分解反应,有电子转移的反应是氧化还原反应;
解答 解:“升炼倭铅”的反应:ZnCO3$\frac{\underline{\;500℃\;}}{\;}$CO2↑+ZnO、CO2+C$\frac{\underline{\;>900℃\;}}{\;}$2CO、ZnO+CO$\frac{\underline{\;>907℃\;}}{\;}$Zn(g)+CO2,
A.Zn易被空气氧化,为防止Zn被氧化而用“泥封”隔绝空气,故A正确
B.“锌火”是未反应完的CO和Zn蒸气从“兜室”逸出燃烧,故B正确;
C.反应区温度达到1100~1300℃,Zn变为蒸气与杂质分离,在“兜室”冷凝为液体流出(冷凝区温度高于Zn的熔点),故C错误;
D.由一种物质生成两种或多种物质的反应是分解反应,有电子转移的反应是氧化还原反应,根据以上分析知,“升炼倭铅”的反应:ZnCO3$\frac{\underline{\;500℃\;}}{\;}$CO2↑+ZnO是分解反应、CO2+C$\frac{\underline{\;>900℃\;}}{\;}$2CO、ZnO+CO$\frac{\underline{\;>907℃\;}}{\;}$Zn(g)+CO2为氧化还原反应,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重考查学生分析判断及获取信息分析问题能力,知道图中发生的反应是解本题关键,题目难度不大.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol--1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知2C(s)+2O2(g)=2CO2(g)△H=a,2C(s)+O2(g)=2CO(g)△H=b,则a>b | |
| C. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3 kJ | |
| D. | 已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
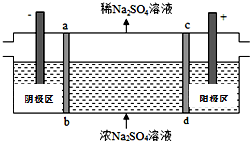 三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )| A. | 通电后中间隔室的SO42-离子向正极迁移,正极区溶液碱性增强 | |
| B. | 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品 | |
| C. | 阴极区溶液pH降低,阳极区溶液pH升高 | |
| D. | 当电路中通过1mol电子的电量时,会有0.5mol的O2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将322 g Na2SO4•10H2O溶于1 L水中,所得溶液的物质的量浓度为1 mol/L | |
| B. | 将含2 mol H2SO4的溶液加水稀释到2 L,所得溶液中H2SO4的物质的量浓度为1 mol/L | |
| C. | 将1 L 18.4 mol/L的H2SO4溶液加入1 L水中,所得溶液的物质的量浓度为9.2 mol/L | |
| D. | 将336 mL HCl气体溶于300 mL水,所得溶液的物质的量浓度为0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
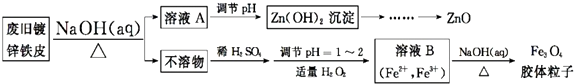
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、NaCl溶于水,破坏的化学键类型相同 | |
| B. | 某物质中含有离子键,则该物质在任何条件下均可导电 | |
| C. | 干冰是分子晶体,其气化过程中只需克服分子间作用力 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验必须使用温度计,且温度计的水银球应在蒸馏烧瓶的支管口处 | |
| B. | 冷凝管中的水流方向是从下口进入,上口排出 | |
| C. | 实验中需要在蒸馏烧瓶中加入几片碎瓷片,防止出现暴沸现象 | |
| D. | 用酒精灯加热时,蒸馏烧瓶必须垫石棉网 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
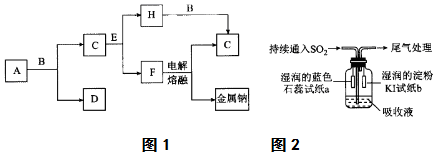
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com