
·ÖĪö £Ø1£©³£ĪĀĻĀ£¬Ä³ČÜŅŗÖŠÓÉĖ®µēĄė²śÉśµÄc£ØH+£©=1”Į10-10mol/L£¬³£ĪĀĻĀ“æĖ®ÖŠĖ®µēĄėµÄĒāĄė×ÓÅضČĪŖc£ØH+£©=1”Į10-7mol/L£¬ĖµĆ÷øĆČÜŅŗÖŠŅÖÖĘĮĖĖ®µÄµēĄė£¬øĆČÜŅŗæÉÄÜĪŖĖįČÜŅŗ»ņÕß¼īČÜŅŗ£¬ĖįČÜŅŗÖŠĒāŃõøłĄė×Ó”¢¼īČÜŅŗÖŠµÄĒāĄė×ÓŹĒĖ®µēĄėµÄ£¬¾Ż“Ė¼ĘĖć³öČÜŅŗÖŠµÄĒāĄė×ÓÅØ¶Č¼°ČÜŅŗµÄpH£»
£Ø2£©øĆČÜŅŗČōĪŖĖįČÜŅŗ£¬ŌņČÜŅŗÖŠĒāŃõøłĄė×ÓŹĒĖ®µēĄėµÄ£¬ČōĪŖŃĪČÜŅŗ£¬ČÜŅŗÖŠĒāĄė×ÓŹĒĖ®µēĄėµÄ£»
£Ø3£©ĮņĖįĒā¼ŲŌŚČÜŅŗÖŠĶźČ«µēĄė³öĒāĄė×Ó”¢¼ŲĄė×ÓŗĶĮņĖįøłĄė×Ó£¬ŌņČÜŅŗĻŌŹ¾ĖįŠŌ£»Ģ¼ĖįĒā¼ŲČÜŅŗÖŠ£¬Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚµēĄė³Ģ¶Č£¬ČÜŅŗ³Ź¼īŠŌ£»ĮņĖįĒā¼ŲÓėĢ¼ĖįĒā¼Ų·“Ӧɜ³ÉĮņĖį¼Ų”¢¶žŃõ»ÆĢ¼ĘųĢåŗĶĖ®£¬¾Ż“ĖŠ“³ö·“Ó¦µÄĄė×Ó·½³ĢŹ½£®
½ā“š ½ā£ŗ£Ø1£©Ė®µēĄėµÄc£ØH+£©=1”Į10-10mol/L£¼c£ØH+£©=1”Į10-7mol/L£¬ĖµĆ÷øĆČÜŅŗŅÖÖĘĮĖĖ®µÄµēĄė£¬ČÜŅŗæÉÄÜĪŖĖįČÜŅŗ»ņ¼īČÜŅŗ£»
ČōĪŖĖįČÜŅŗ£¬ČÜŅŗÖŠµÄĒāĄė×ÓŹĒĖ®µēĄėµÄ£¬Ė®µēĄė²śÉśµÄc£ØH+£©=1”Į10-10mol/L£¬ŌņČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ£ŗc£ØOH-£©=1”Į10-4mol/L£¬ČÜŅŗµÄpH=4£»
ČōĪŖ¼īČÜŅŗ£¬ŌņČÜŅŗÖŠµÄĒāĄė×ÓŹĒĖ®µēĄėµÄ£¬ŌņČÜŅŗÖŠĒāĄė×ÓÅضČĪŖc£ØH+£©=1”Į10-10mol/L£¬ČÜŅŗµÄpH=10£¬
¹Ź“š°øĪŖ£ŗ4»ņ10£»
£Ø2£©Ä³ČÜŅŗµÄpHĪŖ4£¬øĆČÜŅŗæÉÄÜĪŖĖįČÜŅŗ»ņŃĪČÜŅŗ£¬ČōĪŖĖįČÜŅŗ£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓŹĒĖ®µēĄėµÄ£¬ŌņĖ®µēĄėµÄĒāŃõøłĄė×ÓÅضČĪŖ10-10mol/L£»ČōĪŖŃĪČÜŅŗ£¬ŌņČÜŅŗÖŠĒāĄė×ÓŹĒĖ®µēĄėµÄ£¬ŌņĖ®µēĄėµÄĒāŃõøłĄė×ÓÅضČĪŖ10-4mol/L£¬
¹Ź“š°øĪŖ£ŗ10-10mol/L»ņ10-4mol/L£»
£Ø3£©KHSO4ČÜŅŗÖŠµēĄė³öĒāĄė×Ó£¬ČÜŅŗ³ŹĖįŠŌŠŌ£»KHCO3ČÜŅŗÖŠ£¬Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚĘäµēĄė³Ģ¶Č£¬ČÜŅŗĻŌŹ¾¼īŠŌ£¬ČÜŅŗµÄpH£¾7£¬Ė®½āµÄĄė×Ó·½³ĢŹ½±ķŹ¾ĪŖ£ŗHCO3-+H2O?H2CO3+OH-£»ĮņĖįĒā¼ŲÓėĢ¼ĖįĒā¼Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗHCO3-+H+ØTCO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗĖį£»£¾£» HCO3-+H2O?H2CO3+OH-£»HCO3-+H+ØTCO2”ü+H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖĖį¼ī»ģŗĻµÄ¶ØŠŌÅŠ¶Ļ¼°ČÜŅŗpHµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ČÜŅŗĖį¼īŠŌÓėČÜŅŗµÄ¹ŲĻµĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕĖ®µÄµēĄė¼°ĘäÓ°Ļģ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°»Æѧ¼ĘĖćÄÜĮ¦£®


 ŠĀ»ĘøŌ±ų·ØĆܾķĻµĮŠ“š°ø
ŠĀ»ĘøŌ±ų·ØĆܾķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
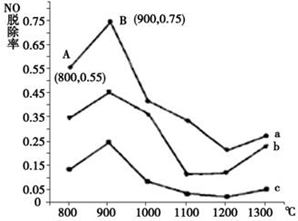 Įņ”¢µŖŃõ»ÆĪļŹĒŠĪ³ÉĖįÓź”¢Īķö²µČ»·¾³ĪŪČ¾µÄ×ļæż»öŹ×£¬²ÉÓĆŗĻŹŹµÄ“ėŹ©Ļū³żĘäĪŪČ¾ŹĒ±£»¤»·¾³µÄÖŲŅŖ¾Ł“ė£®
Įņ”¢µŖŃõ»ÆĪļŹĒŠĪ³ÉĖįÓź”¢Īķö²µČ»·¾³ĪŪČ¾µÄ×ļæż»öŹ×£¬²ÉÓĆŗĻŹŹµÄ“ėŹ©Ļū³żĘäĪŪČ¾ŹĒ±£»¤»·¾³µÄÖŲŅŖ¾Ł“ė£®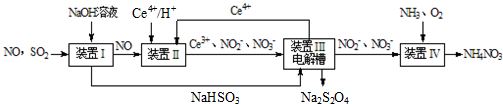
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H”Į+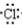 ”ś ”ś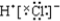 | B£® | Na”Į+ ”ś ”ś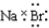 | ||
| C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
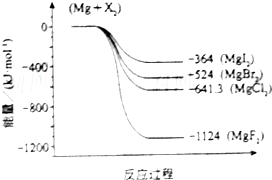 Ć¾»ÆŗĻĪļŗĶĀČĘų¾ł¾ßÓŠ¹ć·ŗÓĆĶ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
Ć¾»ÆŗĻĪļŗĶĀČĘų¾ł¾ßÓŠ¹ć·ŗÓĆĶ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°µŲ¹µÓĶ”±½ūÖ¹Ź³ÓĆ£¬µ«æÉŅŌÓĆĄ“ÖĘ·ŹŌķ | |
| B£® | ĒāŃõ»ÆĀĮ”¢Ģ¼ĖįĒāÄʶ¼æÉÓĆÓŚÖĪĮĘĪøĖį¹ż¶ą | |
| C£® | ĪŖøÄÉĘŹ³ĪļµÄÉ«”¢Ļć”¢Ī¶²¢·ĄÖ¹±äÖŹ£¬æÉŌŚĘäÖŠ¼ÓČėŹŹĮæŹ³Ę·Ģķ¼Ó¼Į | |
| D£® | ÓĆ»ÆĻĖĆęĮĻĢꓜƎ֏ĆęĮĻ£¬ŅŌ¼õÉŁ¶žŃõ»ÆĢ¼µÄÅÅ·Å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĻūŗÄŃĪĖįŅ»Ńł¶ą | B£® | ·Å³öCO2Ņ»Ńł¶ą | ||
| C£® | ĻūŗÄŃĪĖįĒ°Õ߶ą | D£® | ·Å³öµÄCO2£¬µŚŅ»·ŻĪŖµŚ¶ž·ŻµÄŅ»°ė |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņĀČ»ÆŃĒĢśČÜŅŗÖŠĶØČėĀČĘų£ŗFe2++Cl2ØTFe3++2Cl- | |
| B£® | ½«ĀČĘųĶØČėĄäµÄĒāŃõ»ÆÄĘČÜŅŗÖŠ£ŗCl2+2OH-ØTCl-+ClO-+H2O | |
| C£® | °±ĘųĶØČė“×ĖįČÜŅŗCH3COOH+NH3ØTCH3COONH4 | |
| D£® | ½šŹōĀĮČÜÓŚŃĪĖįÖŠ£ŗAl+2H+ØTAl3++H2”ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com