
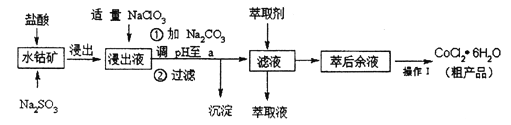
【题目】CoCl2· 6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、 Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2· 6H2O的工艺流程如下:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co (OH) 2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2· 6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中主要发生的离子反应方程式:______________。
(2)若不慎向“浸出液”中加过量NaC1O3时,可能会生成的有害气体是_______(填化学式)。
(3)萃取剂对金属离子的萃取率与pH的关系如图,向“滤液”中加入萃取剂的目的是_______,其使用的最佳pH范围是 ________(选填下列字母)。

A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(4) “操作1”是________。制得的CoCl2· 6H2O需减压烘干的原因是__________。
(5)为测定粗产品中CoCl2· 6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2· 6H2O的质量分数大于100%,其原因可能是___________________。(答一条即可)
【答案】 Co2O3+SO32-+4H+=2Co2++SO42-+2H2O Cl2 除去锰离子 B 蒸发浓缩,冷却结晶,过滤,洗涤,干燥 降低烘干温度,防止产品分解 粗产品含有可溶性氯化物或晶体失去了部分结晶水
【解析】向水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等],加入盐酸和亚硫酸钠,浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等,加入氯酸钠将亚铁离子氧化为Fe3+,然后加入Na2CO3调节pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,过滤后所得滤液经过萃取后主要含有CoCl2,最终得到CoCl26H2O晶体。
(1)向水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等],加入盐酸和亚硫酸钠,浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等,所以Co2O3和亚硫酸钠在酸性条件下发生氧化还原反应,根据电荷守恒和得失电子守恒,反应的离子方程式为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O,故答案为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;
(2)NaClO3的作用是将Fe2+氧化成Fe3+,若不慎向“浸出液”中加过量NaC1O3时,氯酸钠会将本身被还原生成的氯离子氧化,生成氯气,故答案为:Cl2;
(3)根据萃取剂对金属离子的萃取率与pH的关系图,溶液中存在Mn2+、Co2+金属离子,向“滤液”中加入萃取剂可以除去锰离子,在pH为3~4之间时,锰离子的萃取率较高,结合阳离子以氢氧化物形式沉淀时溶液的pH表,可知在pH为3~3.5之间,在可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀,故选B,故答案为:除去锰离子;B;
(4) “操作1”是从溶液中获得溶质的过程,因此“操作1”的步骤为蒸发浓缩,冷却结晶,过滤,洗涤,干燥。根据题意知,CoCl26H2O常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴,为防止其分解,制得的CoCl26H2O需减压烘干,故答案为:蒸发浓缩,冷却结晶,过滤,洗涤,干燥;降低烘干温度,防止产品分解;
(5)根据CoCl26H2O的组成分析,造成产品中CoCl26H2O的质量分数大于100%的原因可能是:含有杂质,导致氯离子含量大或结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大,故答案为:粗产品含有可溶性氯化物或晶体失去了部分结晶水。


科目:高中化学 来源: 题型:
【题目】在逻辑上概念之间存在如图所示关系。对下列概念之间关系的说法正确的是

A. 纯净物与混合物属于包含关系
B. 化合物与氧化物属于交叉关系
C. 单质与化合物属于并列关系
D. 氧化反应与化合反应属于并列关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法正确的是( )

A. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. C(s,石墨)===C(s,金刚石) ΔH=+1.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是从元素周期表中截取的一个片段,其中X,Y,Z,W均属于短周期元素.请回答下列问题.
(1)若X单质为空气中的主要成分之一,则W的原子结构示意图为 .
(2)若Y,W,Z的最高价氧化物对应的水化物依次为一元酸、二元酸、三元酸,这三种酸的正盐的含氧酸根离子中,有两种的电子数相等,这两种离子的离子符号是、 .
(3)若Na与Y和Z的单质分别反应可以生成摩尔质量相同的两种化合物,其中Na与Y形成的化合物的电子式为 , 所含化学键的类型为 .
(4)Y元素在元素周期表中处于第纵行(写出所有可能的纵行数). ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解AgNO3溶液一段时间后,下列有关说法正确的是( )
A. 阳极质量增加
B. 向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况
C. 电解过程中溶液的pH不断升高
D. 电解后两极产生的气体体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的一些物质或概念间的从属关系中,不正确的是( )
X | Y | Z | |
例 | 氧化物 | 化合物 | 纯净物 |
A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
B | 烯烃 | 不饱和烃 | 烃 |
C | 氯乙烷 | 卤代烃 | 烃的衍生物 |
D | 加聚反应 | 加成反应 | 化合反应 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是( )
A.1mol甲基(-CH3)所含的电子总数为8NA
B.0.5mol苯分子中含有C=C双键数为1.5NA
C.11.2L甲醛所含分子数为0.5NA
D.14g乙烯、丙烯的混合气体所含原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m g含氧化铁、氧化铜或氧化亚铁的样品投入到2L物质的量浓度为1mol/L的盐酸中恰好完全反应,若向等质量的该样品中通入足量的氢气并加热,充分反应后所得金属的质量是( )
A.(m﹣16)g
B.(m+16)g
C.(m﹣32)g
D.16g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com