
图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O
对实验现象的“解释或结论”正确的是( )
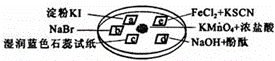
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl﹣ |
|
| A. | A | B. | B | C. | C | D. | D |
| 氯气的化学性质.. | |
| 专题: | 卤族元素. |
| 分析: | Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变红棕色,可证明氧化性:Cl2>I2、Cl2>Br2,无法证明I2与Br2之间氧化性的强弱;C处先变红,说明氯气与水生成酸性物质,后褪色,则证明氯气与水生成具有漂白性物质;d处立即褪色,也可能是氯气与水生成酸性物质中和了NaOH;D处变红说明Cl2将Fe2+氧化为Fe3+,证明还原性:Fe2+>Cl﹣,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl﹣;Fe3++3SCN﹣=Fe(SCN)3;用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO﹣+10OH﹣=2FeO42﹣+3Cl﹣+5H2O. |
| 解答: | 解:A、Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变橙色,可证明氧化性:Cl2>I2、Cl2>Br2,无法证明I2与Br2之间氧化性的强弱,故A错误; B、氯气与水反应Cl2+H2O=H++Cl﹣+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则C处先变红,后褪色,能证明氯气与水生成了酸性物质和漂白性物质,故B错误; C、Cl2和氢氧化钠反应生成氯化钠、次氯酸钠和水,红色褪去可能是因为氢氧化钠被消耗造成,也有可能是生成漂白性物质,故不能证明一定是生成物质具有漂白性,故C错误; D、Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl﹣;Fe3++3SCN﹣=Fe(SCN)3,证明还原性Fe2+>Cl﹣,故D正确; 故选D. |
| 点评: | 本题通过元素化合物知识,考查考生实验能力和对实验现象的分析、推断能力,题目难度中等,注意把握氯气以及其它物质的相关化学性质,把握离子检验方法和特征反应的现象是关键. |


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
如图所示,用铁棒和石墨棒作电极电解1 L 1 mol/L的食盐水,下列有关说法正确的是( )
A.电键K与N连接,铁棒被保护而免受腐蚀
B.电键K与N连接,正极反应式为4OH--4e-===2H2O+O2↑
C.电键K与M连接,当两极共产生标准状况下气体33.6 L时,理论上生成1 mol NaOH
D.电键K与M连接,将石墨棒换成铜棒,就可实现在铁棒上镀铜
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,以下各物质所含分子数最多的是
A.标准状况下11.2 L氯气 B.17g氨气
C.0. 8mol氧气 D.4℃时,36mL的H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是(NA表示阿伏加德罗常数)( )
A.在常温常压下,11.2 升氯气含有的分子数为0.5NA
B.在常温常压下,1摩尔气体含有的原子数为NA
C.32 g氧气所含原子数目为2NA
D.在同温同压下,相同体积的任何气体单质所含原子数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中的少量杂质(杂质不要求回收),把有关的试剂.
操作方法的序号写在相应的括号内。
a. 加适量盐酸,过滤 b.加适量水,过滤蒸发 c.加适量水,过滤
加适量盐酸,过滤 b.加适量水,过滤蒸发 c.加适量水,过滤
d.加热(高温或灼烧) e.加适量盐酸,蒸发 f.冷却热的饱和溶液,过滤
(1)碳酸钙中含有碳酸钠( )
(2)氯化钾粉末中含有碳酸钾( )
(3)氧化钙中含有碳酸钙( )
(4)二氧化锰中含有少量的炭粉( )
(5)硝酸钾中混有少量的食盐( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 |
|
| B. | 向硅酸钠溶液中滴加盐酸,有白色凝胶生成 |
|
| C. | 向AlCl3溶液中逐滴滴加氨水至过量,先出现白色沉淀后溶解 |
|
| D. | 工业上可以电解氯化镁溶液制取金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项表达中正确的是( )
|
| A. | Na2O2的电子式为 |
|
| B. | 106g的乙醇和丙醇混合液完全燃烧生成的CO2为112 L(标准状况) |
|
| C. | 在氮原子中,质子数为7而中子数不一定为7 |
|
| D. | Cl﹣的结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式
A.浓盐酸与铁屑反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
B.Cl2通入水中:Cl2 + H2O = 2H++ Cl-+ ClO-
C.往稀硫酸中滴入氢氧化钡溶液:Ba2++SO42-=BaSO4↓
D.实验室制备二氧化碳气体: 2H+ + CaCO3 ═ Ca2+ + CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
将含有等体积NH3、CO2、NO的混合气体依次通过盛有浓硫酸、Na2O2和Na2CO3溶液的装置,充分作用后,最后得到的气体是( )
A.CO2和NO B.CO2
C.NO D.NO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com