
| ||
| ||
| ||
| ||
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
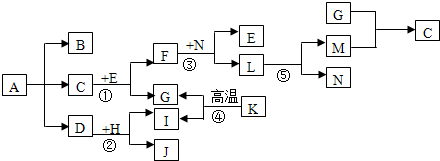
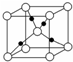 X、R、W、Y、Z是元素周期表中前四周期的五种元素,其原子序数依次增大,其中X、R、W同周期,X和Y同一主族.X原子最外层的p轨道上的电子数等于前一电子层上的电子总数,W原子最外层的p轨道中只有一个轨道填充了2个电子.Z的单质是一种紫红色金属,Z可与W形成Z2W、ZW等化合物.根据上述信息回答下列问题:
X、R、W、Y、Z是元素周期表中前四周期的五种元素,其原子序数依次增大,其中X、R、W同周期,X和Y同一主族.X原子最外层的p轨道上的电子数等于前一电子层上的电子总数,W原子最外层的p轨道中只有一个轨道填充了2个电子.Z的单质是一种紫红色金属,Z可与W形成Z2W、ZW等化合物.根据上述信息回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
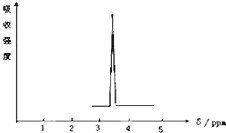 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用pH试纸鉴别乙醇和乙酸 |
| B、用食醋浸泡有水垢的水壶清除其中的水垢 |
| C、用乙醇从碘水中萃取碘 |
| D、用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ | ||||
| B、双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O | ||||
C、用铜做电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| D、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com