
某研究性学习小组为研究光化学烟雾消长规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2)及各种物质的相对浓度随时间的变化,记录于图中。根据图中数据,下列推论最不合理的是( )
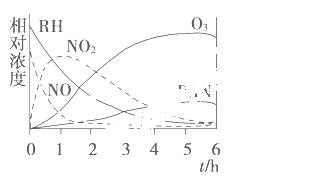
A.NO消失的速率比RH快
B.NO生成NO2
C.RH及NO2反应生成PAN及O3
D.O3生成PAN
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意图如下:

(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
Fe+2Fe3+===3Fe2+
2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O===TiO2+(无色)+Fe2++2H+
加入铁屑的作用是____________________________________________ ______________
______________
________________________________________________________________________。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在________范围。
 (3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=________。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=________。
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g)
ΔH=+140 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是__________________(只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用________方法。
| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.6 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于电解质溶液的判断正确的是 ( )
A.60 ℃时,NaCl溶液的pH<7,则溶液中c(OH-)<c(H+)
B.将pH=4的CH3COOH溶液加水稀释,溶液中所有离子的浓度均减小
C.常温下,CH3COOH分子可能存在于pH>7的碱性溶液中
D.相同温度下,1 mol·L-1氨水与0.5 mol·L-1氨水中c(OH-)之比是2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
对于0.1 mol·L-1的Na2S溶液,下列判断正确的是 ( )
A.溶液中阴离子浓度的大小顺序:c(S2-)>c(OH-)>c(HS-)
B.c(Na+)=2c(S2-)+c(OH-)+c(HS-)
C.c(OH-)=c(H+)
D.向溶液中加入少量NaHS固体,溶液中的离子种数增多
查看答案和解析>>
科目:高中化学 来源: 题型:
启普发生器是一种具有能即时开、关(以便能即时产生或停止产生气体)功能的气体发生器,下列装置(支持装置部分省略了)制备相应气体时不具备上述功能的是( )
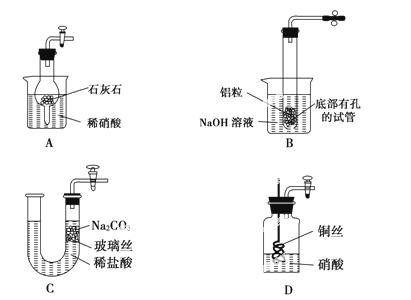
查看答案和解析>>
科目:高中化学 来源: 题型:
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )

A.溴酸银的溶解时放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O.当有1mol H2O参与反应时,转移电子的物质的量为( )
|
| A. | 0.5 mol | B. | 1 mol | C. | 2 mol | D. | 4 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com