
| A. | 该反应的正反应是放热反应 | |
| B. | 若在第6 min时升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| C. | 图a中反应达到平衡时,Y的转化率为37.5% | |
| D. | 反应中某时刻各物质的正反应速率为2v(X)═2v(Y)═v(Z) |
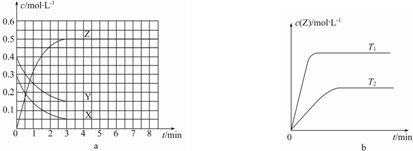
分析 根据图a知,X、Y是反应物而Z是生成物,
A.图b中,根据“先拐先平数值大”知,T1>T2,升高温度,Z的含量增大,说明平衡正向移动,升高温度平衡向吸热反应方向移动;
B.该反应的正反应是吸热反应,升高温度,正逆反应速率都增大,平衡正向移动;
C.转化率=$\frac{参加反应的浓度变化量}{反应初始浓度}×100%$;
D.参加反应的△c(X)=(0.3-0.05)mol/L=0.25mol/L、△c(Y)=(0.4-0.15)mol/L=0.25mol/L、△c(Z)=(0.5-0)mol/L=0.5mol/L,同一反应同一时间段内各物质的浓度变化量之比等于反应速率之比.
解答 解:根据图a知,X、Y是反应物而Z是生成物,
A.图b中,根据“先拐先平数值大”知,T1>T2,升高温度平衡向吸热反应方向移动,升高温度,Z的含量增大,说明平衡正向移动,所以正反应是吸热反应,故A错误;
B.该反应的正反应是吸热反应,升高温度,正逆反应速率都增大,但正反应速率增大程度大于逆反应速率,所以平衡正向移动,故B错误;
C.转化率=$\frac{参加反应的浓度变化量}{反应初始浓度}×100%$=$\frac{(0.4-0.15)mol/L}{0.4mol/L}×100%$=62.5%,故C错误;
D.参加反应的△c(X)=(0.3-0.05)mol/L=0.25mol/L、△c(Y)=(0.4-0.15)mol/L=0.25mol/L、△c(Z)=(0.5-0)mol/L=0.5mol/L,同一反应同一时间段内各物质的浓度变化量之比等于其反应速率之比,所以X、Y、Z的反应速率之比=0.25mol/L:0.25mol/L:0.5mol/L=1:1:2,即反应中某时刻各物质的正反应速率为2v(X)═2v(Y)═v(Z),故D正确;
故选D.
点评 本题以图象分析为载体考查化学平衡计算,侧重考查学生分析计算能力,根据“先拐先平数值大”判断温度高低从而确定反应热,知道反应中各物质反应速率与计算数的关系,题目难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:解答题
 乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示)填空:
乙二酸俗称草酸是一种二元弱酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示)填空:| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
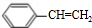 ,A分子中处于同一平面的原子最多有16个;
,A分子中处于同一平面的原子最多有16个;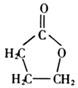 :
: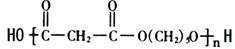 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 暴雨后遭洪水浸泡的铁门生锈是因为发生化学腐蚀 | |
| B. | 白铁皮(铁镀锌)表面有划损时,不能阻止铁被腐蚀 | |
| C. | 废弃的干电池不能随意丢弃,但可以土埋处理 | |
| D. | 不能将铁制自来水管与铜制水龙头连接 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫不能使溴水、高锰酸钾溶液迅速褪色 | |
| B. | 接触法制硫酸的沸腾炉排出的炉气中含SO2 | |
| C. | 实验室可用启普发生器制取二氧化硫 | |
| D. | 用石灰水很容易区分二氧化碳和二氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸与碳酸钠溶液反应的离子方程式:2H++CO32-═CO2↑+H2O | |
| B. | 苯酚钠溶液中通入少量二氧化碳的离子方程式:2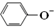 +H2O+CO2→2 +H2O+CO2→2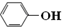 +CO32- +CO32- | |
| C. | 丙烯聚合成聚丙烯的化学方程式:nCH2=CHCH3$\stackrel{催化剂}{→}$  | |
| D. | 乙醛溶液与足量的银氨溶液共热的化学方程式:CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com