
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
族 周期 |
I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
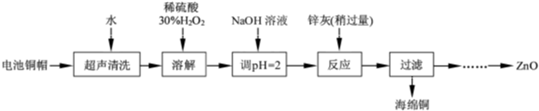
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
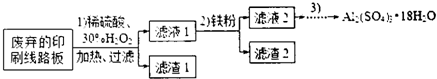
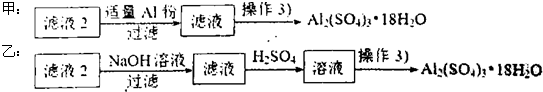
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.8 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了四种溶液溶质的质量分数和物质的量浓度数值:
| 溶质 | HCl | HNO3 | CH3COOH | NaOH |
| 溶质的质 量分数/% | 36.5 | 63 | 40 | 40 |
| 物质的量浓 度/mol·L-1 | 11.8 | 13.8 | 10.6 | 14.3 |
则各溶液中密度最小的是()
A.HCl B.HNO3
C.CH3COOH D.NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com