
 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).分析 (1)已知:①C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1
②CH3CH=CH2(g)═CH4(g)+HC≡CH(g )△H2=32.4kJ•mol-1
根据盖斯定律,①-②得目标热化学方程式;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,以此来书写电池总反应方程式,原电池中阴离子向负极移动;
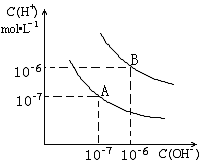
(3)H2CO3?HCO3-+H+的平衡常数Ka=$\frac{c({H}^{+})×c(HC{{O}_{3}}^{-})\;}{c({H}_{2}C{O}_{3})\;}$,利用忽略水的电离及H2CO3的第二级电离,由溶液的pH=5.60可知c(H+),然后代入计算.
解答 解:(1)已知:①C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1
②CH3CH=CH2(g)═CH4(g)+HC≡CH(g )△H2=32.4kJ•mol-1
根据盖斯定律,①-②得C3H8(g)═CH3CH=CH2(g)+H2(g),所以△H=△H1-△H2=156.6kJ•mol-1-32.4kJ•mol-1=124.2kJ•mol-1;
故答案为:124.2;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,即丙烷与氧气反应生成二氧化碳和水,则电池的总反应为C3H8+5O2═3CO2+4H2O,原电池中阴离子向负极移动,即CO32-移向电池的负极,故答案为:C3H8+5O2═3CO2+4H2O;负;
(3)忽略水的电离及H2CO3的第二级电离,pH=5.60,c(H+)=10-5.60=2.5×10-6mol•L-1,
由H2CO3?HCO3-+H+,
平衡时c(H+)=c(HCO3-)=2.5×10-6mol•L-1,
c(H2CO3)=(1.5×10-5-2.5×10-6)mol•L-1,
则Ka=$\frac{c({H}^{+})×c(HC{{O}_{3}}^{-})\;}{c({H}_{2}C{O}_{3})\;}$=4.2×10-7 mol•L-1,
故答案为:4.2×10-7 mol•L-1.
点评 本题考查较为综合,为高频考点,侧重考查学生的分析能力和计算能力,明确盖斯定律、原电池的工作原理、电离平衡常数的计算、溶液中利用电离与水解来比较离子的浓度即可解答,难度不大.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:解答题
| 操作过程 | 实验现象描述 | 对应离子方程式或化学方程式 |
| FeCl2中通入Cl2 | 溶液变黄 | 2Fe2++Cl2=2Fe3+ |
| Fe(OH)2放置空气 | 白色沉淀迅速变为灰绿色,最终变为红褐色 | 4Fe(OH)2+O2+4H2O=4Fe(OH)3 |
| KI溶液中通入氯气,加入CCl4后震荡 | 溶液变为棕色,加入四氯化碳后分层,且四氯化碳层显紫色 | Cl2+2I-=2Cl-+I2 |
| 盐酸溶液中缓慢滴加Na[Al(OH)4]溶液至过量 | 先无沉淀,后生成白色沉淀 | [Al(OH)4]-+4H+=Al3++4H2O,3[Al(OH)4]-+Al3+=4Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体2是氧化铁 | |
| B. | X的化学式可以表示为Fe3C2 | |
| C. | 溶液甲中可能含有Fe3+ | |
| D. | X与足量的热浓硝酸反应有NO2和CO2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
| A. | NH4+-气体法 | B. | I--沉淀法 | ||
| C. | Na+-显色法 | D. | CO32--气体法和沉淀法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
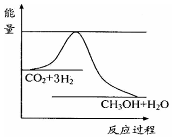 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠:供氧剂 | B. | 碱石灰:干燥剂 | ||
| C. | 小苏打:发酵粉主要成分 | D. | 纯碱:治疗胃酸过多的一种药剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10种 | B. | 9种 | C. | 8种 | D. | 7种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com