
| A. | 石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 煤干馏和石油分馏本质差别是:干馏是化学变化而分馏是物理变化 | |
| D. | 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
分析 A.汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在C5~C11范围内;
B.含C18以上烷烃的重油经过催化裂化可得到汽油、煤油和柴油;
C.煤的干馏有新物质生成,石油的分馏是利用沸点不同来分离混合物;
D.煤中不含苯和甲苯.
解答 解:A.石油中含有C5-C11的烷烃,可以通过石油的分馏得到汽油,其分子中的碳原子数一般在C5~C11范围内,故A正确;
B.含C18以上烷烃的重油经过催化裂化可得到汽油、煤油和柴油等轻质油,能提高汽油的产量,故B正确;
C.煤的干馏是指煤在隔绝空气的条件下加热,生成煤焦油、焦炭、焦炉煤气等物质,属于化学变化.石油分馏是指通过石油中含有的物质的沸点不同而使各种物质分离开的一种方法,该过程中没有新物质生成,属于物理变化,故C正确;
D.煤中不含苯和甲苯,苯和甲苯是煤经过分馏生成的,而不是煤本身含有的,故D错误.
故选D.
点评 本题考查化石燃料的综合利用,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 容器内压强不随时间变化 | |
| B. | v正(X)=v逆(Z) | |
| C. | 容器内X、Y、Z的浓度之比为l:2:2 | |
| D. | 单位时间内消耗0.1 mol X的同时生成0.2 mol Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验用剩的药品应放回原试剂瓶中 | |
| B. | 切割白磷时应该在水下进行 | |
| C. | 测某酸性溶液的pH时,先用水将pH试纸湿润 | |
| D. | 在“粗盐中难溶性杂质的去除”实验中,将蒸发皿中的溶液直接蒸干 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含共价键的物质一定是共价化合物 | |
| B. | HF、HCl、HBr、HI沸点逐渐增加是因为分子量逐渐增加 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 金属与非金属之间形成的是离子键,非金属之间则形成的是共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该混盐具有和漂白粉相似的化学性质 | |
| B. | 该混盐的水溶液呈中性 | |
| C. | 该混盐与硫酸反应生成1摩尔氯气时,转移了1摩尔电子 | |
| D. | 该混盐中氯元素的化合价为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
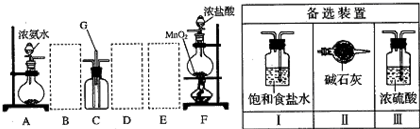
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
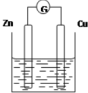 如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com