
【题目】某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

A.由图甲推断,B点SO2的平衡浓度为0.3 mol·L-1
B.由图甲推断,A点对应温度下该反应的平衡常数为800L·mol-1
C.压强为0.50 MPa时不同温度下SO2转化率与温度关系如乙图,则T2>T1
D.达平衡后,若增大容器容积,则反应速率变化图像可以用图丙表示
【答案】B
【解析】
由图甲可知增大压强二氧化硫的转化率增大,平衡正向移动;先拐先平衡,数据越大,因而图乙中可知温度T1>T2;又因反应为放热反应,升高温度平衡向着吸热的方向移动,因此升高温度平衡逆向移动,结合以上分析进行判断并计算。
A. 设B点SO2的转化量为x mol,根据三段法可知:
2SO2(g) + O2(g) ![]() 2SO3(g)
2SO3(g)
始(mol) 2 1 0
转(mol) x ![]() x
x
平(mol) 2-x 1- ![]() x
x ![]() =0.85 x=1.7mol
=0.85 x=1.7mol
平衡时SO2的平衡浓度为![]() =0.03mol/L,A项错误;
=0.03mol/L,A项错误;
B. 设A点O2的转化量为y mol,根据三段法可知:
2SO2(g) + O2(g) ![]() 2SO3(g)
2SO3(g)
始(mol/L) 0.2 0.1 0
转(mol/L) 2y y 2y
平(mol/L) 0.2-2y 0.1-y 2y ![]() =0.80 y=0.08mol/L
=0.80 y=0.08mol/L
平衡常数K= =800 L·mol-1,B项正确;
=800 L·mol-1,B项正确;
C. 先拐先平衡,数据越大,因而图乙中T1>T2,C项错误;
D. 达平衡后,若增大容器容积,相当于减小压强,反应速率减慢,平衡逆向移动,v(逆)>v(正),因此不能用图丙表示,D项错误;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】最近,科学家开发出一种低成本光伏材料——蜂窝状石墨烯。生产原理是:Na2O+2CO Na2CO3+C(石墨烯),然后除去Na2CO3,即可制得蜂窝状石墨烯。下列说法不正确的是
Na2CO3+C(石墨烯),然后除去Na2CO3,即可制得蜂窝状石墨烯。下列说法不正确的是
A.石墨烯与金刚石互为同素异形体
B.该生产石墨烯的反应中CO只体现了还原性
C.Na2O属于碱性氧化物,Na2CO3属于盐
D.自然界中碳元素有游离态和化合态两种存在形式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu的单质和合金在生活、生产中有着广泛的应用。回答下列问题:
(1)Cu的基态原子价电子排布式为___。
(2)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是___,反应的化学方程式为___。
(3)配离子Cu(CN)32-中,中心离子的杂化类型是___,该配离子的空间构型为___;CN-中配位原子是___(填名称)。
(4)CaCux合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。(a)是由Cu和Ca共同组成的层,层中Cu—Cu之间由实线相连;(b)是完全由Cu原子组成的层,Cu—Cu之间也由实线相连。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成CaCux合金的晶体结构图。在这种结构中,同一层的Ca—Cu距离为294pm,相邻两层的Ca—Cu距离为327pm。
①该晶胞中Ca有___个Cu原子配位(不一定要等距最近)。
②同一层中,Ca原子之间的最短距离是___pm,设NA为阿伏加德罗常数的值,CaCu晶体的密度是___g/cm3(用含m、n的式子表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4molA和 2molB进行如下反应:3A(g)+2B(g)![]() 4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6molC,则下列说法正确的是( )
4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6molC,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是 K=![]()
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加 B,平衡向右移动,B的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是
A.5. 6 L由CO2和O2组成的混合气体中的分子数为0. 25NA
B.5. 6 g铁与足量的稀硫酸完全反应转移的电子数为0. 2NA
C.0. 5 mol L-1的BaCl2溶液中含有Cl-的数目为NA
D.10 g质量分数为17%的H2O2溶液中含氧原子的数目为0. 1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质① H2O和D2O ②乙烷和庚烷 ③ CH3CH2CH2CH3 和 (CH3)2CHCH3 ④ 12C和14C ⑤C2H4和C3H6 ⑥ CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5 ⑦金刚石和石墨 ⑧![]() 和
和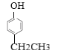
互为同系物的是____________;(填序号,下同)互为同分异构体的是____________;
是同一物质的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质。首先做了银镜反应:
(1)取少量甲酸加入NaOH溶液中和其酸性,反应的离子方程式为_________________。
(2)在(1)的溶液中加入足量银氨溶液,加热,产生了银镜。甲酸钠溶液与银氨溶液发生银镜反应的离子方程式为_______________________________________________。
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作_________________(写字母):
A.用洁净的试管 B.向银氨溶液中加入硝酸酸化
C.用前几天配制好的银氨溶液 D.直接在银氨溶液里加入稍过量的甲酸;
E.在浓度为2%的NH3H2O中滴入稍过量的浓度为2%的硝酸银
然后,同学们对甲酸与甲醇的酯化反应进行了研究:
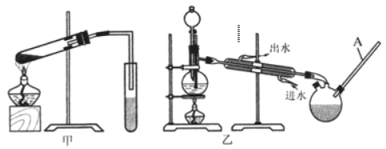
(4)写出![]() 和CH3-18OH进行酯化反应的化学方程式______________________。
和CH3-18OH进行酯化反应的化学方程式______________________。
(5)你认为选择甲装置还是乙装置好?_______,原因是______________________。乙装置中长导管C的作用是_________________。
(6)实验中饱和碳酸钠溶液的作用是_____________________________。从饱和碳酸钠溶液中分离出酯需要用到的主要实验仪器是_______________。
(7)一同学用装有饱和氢氧化钠的三颈烧瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时下列物质的溶度积
CH3COOAg | AgCl | AgCrO4 | AgS | |
Ksp | 2.3×10-3 | 1.77×10-10 | 1.12×10-12 | 6.7×10-15 |
下列说法正确的是( )
A.等体积浓度均为0.02molL-1的CH3COONa和AgNO3溶液混合能产生沉淀
B.浓度均为0.01molL-1的CrO42-和Cl-混合溶液中慢慢滴入AgNO3溶液时,CrO42-先沉淀
C.在CH3COOAg悬浊液中加入盐酸发生反应的离子方程式:CH3COOAg+H++C1-=CH3COOH+AgCl
D.298K时,上述四种饱和溶液的物质的量浓度:c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高分子材料的结构如图所示: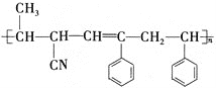 ,已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是
,已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是
A.合成该高分子的反应是缩聚反应
B.形成该高分子材料的单体![]() 中,所有原子可能处于同一平面内
中,所有原子可能处于同一平面内
C.三种单体中有两种有机物互为同系物
D.三种单体都可以使溴水褪色,但只有两种能使酸性高锰酸钾溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com