
【题目】下面列出了几组物质,请将物质的合适序号填写在横线上。
① O2和O3② CH3CH3和CH3CH2CH2CH3 ③![]() 和
和![]()
④ CH3CH(CH3)CH2CH3和C(CH3)4 
(1) 属于同位素的是: (2) 属于同素异形体的是:
(3) 属于同系物的是: (4) 属于同分异构体的是:
(5) 属于同一物质: 。
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】浓硫酸具有性质有 A.强酸性,B.强氧化性,C.高沸点、难挥发性,D.脱水性,E.吸水性。以下过程主要表现了浓硫酸的哪些性质?请将答案的字母分别填入括号中。
(1)用NaCl固体和浓硫酸在加热条件下制氯化氢气体____________
(2)用磷矿物[主要成分是Ca3(PO4)2]和硫酸反应制磷酸____________
(3)浓硫酸干燥H2、O2、Cl2、HCl和SO2等气体____________
(4)常温下可以用铁或铝的容器贮存浓硫酸____________
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末____________
(6)不能用浓硫酸干燥HBr、HI和H2S等气体____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物在生活中无处不在,对人类的生产生活有着重要的作用。
(1)下列物质中不属于有机物的是_____(填字母)。
a.CO2 b.CH4 c.CH3COOH
(2)下列有机物不属于合成高分子的是_____(填字母)。
a.塑料 b.聚乙烯 c.蛋白质
(3)下列物质中不属于糖类的是_____(填字母)。
a.淀粉 b.氨基酸 c.纤维素
(4)下列不属于油脂水解产物的是_____(填字母)。
a.高级脂肪酸 b.甘油(丙三醇) c.乙烯
(5)下列物质中的组成元素与另两种不同的是_____(填字母)。
a.蛋白质 b.糖类 c.油脂
(6)蔗糖的水解产物是_____、_____(填名称),淀粉的化学式为_____。
(7)写出乙烯与溴水反应的化学方程式:_____,该反应类型为_____反应。
(8)乙醇能使酸性KMnO4溶液褪色,这是因为乙醇具有_____性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减少雾霾天气,大容量的镍氢电池已经开始用于汽油/电动混合动力汽车上。镍氢电池放电时的电极反应为:H2+2OH--2e-=2H2O,NiO(OH)+H2O+e-=Ni(OH)2+OH-。下列说法正确的是
A.电池放电时,H2发生还原反应B.电池放电时,Ni(OH)2发生氧化反应
C.电池充电时,H2O发生还原反应.D.电池充电时,NiO(OH)发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NH2COO-+2H2O![]() HCO3-+NH3˙H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是
HCO3-+NH3˙H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是

A.无法判断T1和T2的大小关系
B.T1℃时,第6min反应物转化率为6.25%
C.T2℃时,0~6minν(NH2COO-)=0.3molL-1min-1
D.往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A,相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢直接相连。A在一定条件下氧化只生成G,G能使石蕊试液变红。
已知:![]() 试写出:
试写出:
(1)A的分子式: 。
(2)化合物A和G的结构简式:A ,G
(3)与G同类的同分异构体(含G)可能有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:(无特殊说明均填元素符号、化学式等化学用语)
主族 | IA | ⅡA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | |||
3 | ⑦ | ⑧ | ⑨ | |||||
4 | ⑩ |
(1)在这些元素中,化学性质最不活泼的是 ,元素原子半径最小的是 ,被称为“国防金属”的是 ,可作为半导体材料的是 ,单质氧化性最强的元素是 。
(2)元素②的一种同位素(含8个中子)可测定文物年代,这种同位素的符号是 。
(3)在上述元素的最高价氧化物对应水化物中,碱性最强的化合物的化学式是 。酸性最强的化合物的化学式是 。
(4)写出③的气态氢化物与其最高价氧化物对应水化物反应的方程式 。
(5)元素④的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)欲从苯酚的乙醇溶液中回收苯酚,有下列操作,合理的顺序是 (填字母)。
①蒸馏 ②过滤 ③静置分液 ④加入足量金属钠 ⑤通入过量CO2
⑥加入足量NaOH 溶液 ⑦加入足量FeCl3溶液 ⑧加入足量浓溴水
A. ⑧ ② B.⑥ ① ⑤ ③ C.④② D.⑦ ① ③
(2)下列说法正确的是 (填序号)。
①麦芽糖及其水解产物均能发生银镜反应,且试管内壁的银镜需用稀氨水洗涤
②蛋白质溶液中加入饱和硫酸铵溶液,有沉淀析出,加水后沉淀也不溶解
③淀粉液中加入几滴稀硫酸加热几分钟,冷却后加入银氨溶液并水浴加热,没有观察到银镜现象,证明淀粉未发生水解
④只用溴水就能鉴别四氯化碳、甲苯、乙烯、乙醇
Ⅱ已知:CH3CH2OH+NaBr+H2SO4(浓) ![]() CH3CH2Br+NaHSO4 +H2O。
CH3CH2Br+NaHSO4 +H2O。
实验室制备溴乙烷(沸点为38.4℃)的装置如图:圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的10.3g溴化钠和几粒碎瓷片,小火加热,使NaBr充分反应。
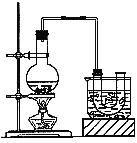
(1)反应时若温度过高会降低溴乙烷的产率,原因是 ;也可看到有红棕色气体产生,该气体的化学式为 。为避免温度过高,宜采用 加热。
(2)反应结束后,U形管中粗制的溴乙烷呈棕黄色。为了除去其中的杂质,最好选用下列试剂中的
(填序号)。
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
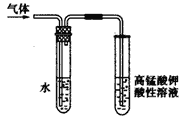
(3)溴乙烷在NaOH水溶液和NaOH乙醇溶液发生不同类型的反应,生成不同的产物,用右图所示装置进行实验:该实验的目的是 。 盛水的试管(装置)的作用是 。
(4)为检验溴乙烷中的溴元素,正确的操作顺序是:取少量溴乙烷,然后 (填序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液 ⑤冷却
(5)经提纯最终得到纯净的溴乙烷为7.63g,则溴乙烷的产率为 (保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了保护环境,科学家们着力研究大气污染物的治理。
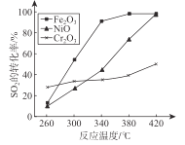
(1)治理含CO、SO2的烟道气以Fe2O3做催化剂,将CO、SO2在380℃时转化为S和一种无毒气体。已知:①硫的熔点:112.8℃、沸点:444.6℃;于反应每得到mol硫,放出 270kJ的热量。写出该治理烟道气反应的热化学方程式____________________________________;其他条件相同、催化剂不同时,上述反应中SO2的转化率随反应温度的变化如图所示,不考虑催化剂价格因素,生产中选Fe2O3做催化剂的主要原因是 ____________________________________;
(2)在450℃,并有V2O5的催化剂存在下SO2能转化为SO3:2SO2(g)+O2 (g)![]() 2SO3(g) △H= -190kJ·mol -1;已知单质硫的燃烧热为296kJ·mol -1,则 S(s)+
2SO3(g) △H= -190kJ·mol -1;已知单质硫的燃烧热为296kJ·mol -1,则 S(s)+![]() O2(g)
O2(g)![]() SO3(g) △H=___kJ·mol -1 。在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:2SO2+2nCu+(n+1)O2+(2-2n)H2O =2nCuSO4 +(2-2n)H2SO4 从环境保护的角度看,催化脱硫的意义为__________;每吸收标准状况下11.2 LSO2,被SO2还原的O2的质量为__________g。
SO3(g) △H=___kJ·mol -1 。在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:2SO2+2nCu+(n+1)O2+(2-2n)H2O =2nCuSO4 +(2-2n)H2SO4 从环境保护的角度看,催化脱硫的意义为__________;每吸收标准状况下11.2 LSO2,被SO2还原的O2的质量为__________g。
(3)在一个固定容积为5L的密闭容器中充0.20molSO2和0.10molO2,在450℃并有催化剂条件下,半分钟后达到平衡,测得容器中含SO30.10 mol,则V(O2)=______(mol·L -1·min -1 );放出的热量为______kJ;该温度下的平衡常数为________;若继续通入0.20 molSO2和0.10mol O2,则再次平衡时,二氧化硫的转化率________(选填“变大”、“变小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com