
某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:

该实验的主要操作步骤如下:
①配制100 mL 1.0 mol·L-1的盐酸溶液;
②用________(填仪器名称并注明规格)量取7.5mL 1.0 mol·L-1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)步骤①中,配制100 mL 1.0 mol·L-1的盐酸溶液时,下列哪些操作会使配制浓度偏小(填写字母) 。
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤②_______________ 步骤③___________
(3)实验步骤⑤中应选用__________(填字母)的量筒。
A.100 mL B.200 mL C.500 mL
(4)读数时除恢复到室温外,还要注意
①______________________________,②_________________________________。
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=____L/mol。
【知识点】一定浓度的溶液的配置,气体摩尔体积的计算 J5 A3 A2
【答案解析】(1)A C (2)②10 mL量筒 ③0.090(未保留两位有效数字扣一分)
(3)A (4)调节量筒高度,使量筒内的液面与集气瓶内的液面相平 ;读数时眼睛视线应与量筒中水的凹液面相平
(5)4/15 V(或者1/3.75V,不能使用数字表示,使用数字表示一律算错误)
解析:(1)A.用量筒量取浓盐酸时,俯视量筒的刻度会使所量取溶液的体积减小,时所配置的溶液的浓度偏小; B.容量瓶未干燥即用来配制溶液对所配置的溶液的浓度没有影响;C.浓盐酸在烧杯中稀释时,搅拌时间过长会使盐酸溶液中的溶质挥发使所配置的溶液的浓度偏低;D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线不会对所配置的溶液的浓度有影响;E.在容量瓶中定容时俯视容量瓶刻度线会使容量瓶中的液体的体积偏小,所配置的溶液浓度偏大;F.烧杯中有少量水对配置的溶液的浓度无关。
②题中要求酸的体积7.5mL,故选用10mL量筒即可。
③Mg+2HCl═MgCl2+H2↑
1mol 2mol
n 0.0075 mol
n=0.00375mol 故a=24g/mol×0.00375mol =0.090
(3)Mg+2HCl═MgCl2+H2↑
2mol 1mol
0.0075 mol n(H2)
n(H2)=0.00375mol V(H2)=0.00375 mol×22.4L/mol=0.056L=56ml,应选100mL量筒,
(4)读数时要保持左右气体压强相等,以减少误差,故应注意:将量筒缓缓向下移动,使乙、丙中液面相平;
(5)由(2)得气体的物质的量为0.00375 mol,通过⑥的气体的体积为V mL,Vm=V/n=0.001VmL/0.00375 mol=1/3.75 V L/mol,
【思路点拨】本题主要考查了一定体积的一定浓度的溶液的配置,在配置过程中要注意的一些事项都在本题中有所考查,气体摩尔体积的计算要抓住定义进行计算即可,试题的综合性较强。


科目:高中化学 来源: 题型:
在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试计算:
(1)O2的转化率为
(2)用SO2表示该反应的反应速率为
(3)平衡时容器内气体压强与反应前的压强之比为 (最简整数比)
(4)平衡时体系中SO3的百分含量(体积分数)为
(5)平衡常数K的值为
查看答案和解析>>
科目:高中化学 来源: 题型:
在V mL Al2(SO4)3溶液中含有Al3+m g,取V/4 mL该溶液用水稀释至4V mL,则SO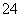 物质的量浓度为 ( )
物质的量浓度为 ( )
A.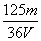 mol/L B.
mol/L B.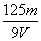 mol/L C.
mol/L C.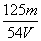 mol/L D.
mol/L D.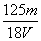 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
某乙醇水溶液的质量分数为w%,物质的量浓度为cmol/L ,密度为dg/mL,1Kg这种溶液中含有的乙醇是:
,密度为dg/mL,1Kg这种溶液中含有的乙醇是:
A.46C g B.c/d mol C.c mol D.1000dw g
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验不能达到预期实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将2.5 g CuSO4·5H2O溶解在97.5 g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1 mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 取少量待检固体溶于水中,滴加少量Ba(OH)2溶液,观察是否有白色沉淀生成 | 检验NaHCO3固体中是否含Na2CO3 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质分类正确的是
A.SO2、SiO2、 CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
生活和生产中常用到胶体的性质,请看下述三例:
(1)医学上治疗由肾功能衰竭等疾病引起的血液中毒时,最常用的血液 净化手段是血液透析。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。透析原理同胶体的________类似,透析膜同________类似,透析膜的孔径应________(填“大于”“小于”或“等于”)血液内毒性物质粒子的直径,毒性物质才可能扩散到透析液中而被除去。
净化手段是血液透析。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。透析原理同胶体的________类似,透析膜同________类似,透析膜的孔径应________(填“大于”“小于”或“等于”)血液内毒性物质粒子的直径,毒性物质才可能扩散到透析液中而被除去。
(2)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量的情况。解决方法之一是把这些陶土和水一起搅拌,使微粒直径在10-9~10-7m之间,然后插入两根电极,再接通直流电源。这时,阳极聚集_______,阴极聚集________,理由是______________________________。
(3)水泥和冶金工厂常用高压电对气溶胶作用除去大量烟尘,以减少对空气的污染,这种 做法运用了________原理。
做法运用了________原理。
查看答案和解析>>
科目:高中化学 来源: 题型:
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5的酸碱性为 ,试样的pH值 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:H2(g)+1/2O2(g)=H2O(g)  H= -241.8KJ/mol
H= -241.8KJ/mol
C(s)+1/2O2(g)=CO(g)  H= -110.5KJ/mol
H= -110.5KJ/mol
写出焦炭与水蒸气反应的热化学方程式 ;
②洗涤含SO2的烟气,以下物质可作洗涤剂的是 ;
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g)
2NO(g)  H>0
H>0
若1mol空 气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol.计算该温度下的平衡常数K= ___________;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是
气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol.计算该温度下的平衡常数K= ___________;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是  。
。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g)已知该反应的 H>
H> 0,简述该设想能否实现的依据 。
0,简述该设想能否实现的依据 。
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com