
利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a处溶液的pH增大,b处溶液的pH减小
D.a、b两处具有相同的电极反应式:Fe-2e-=Fe2+

 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
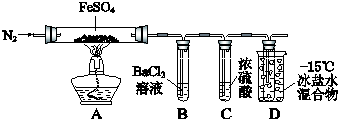
| 实验过程 | 实验现象 | |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
查看答案和解析>>
科目:高中化学 来源:2013届北京市西城区高三上学期期末考试化学试卷(带解析) 题型:实验题
(8分)某小组取一定质量的FeSO4固体,利用下图装置进行实验。
| | 实验过程 | 实验现象 |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年福建省泉州市高三质检理综化学试卷(解析版) 题型:填空题
无水硝酸铜极易吸水,加热到210℃升华,它和Cu(NO3)2 ·3H2O晶体的化学性质有较大差异, Cu(NO3)2 ·3H2O晶体加热到170℃分解。已知:乙酸乙酯的沸点为77 ℃。
(1)加热蒸干Cu(NO3)2 溶液得不到无水硝酸铜的原因是_____________。
(2)将铜片加人到N2 O 4的乙酸乙酯溶液中可制得无水硝酸铜,同时生成NO,写出反应的化学方程式_____________;从乙酸乙醋中分离出无水硝酸铜的实验操作是_____________。
(3)为探究Cu(NO3)2 ·3H2O受热分解的产物,某探究小组利用下图装置进行实验。(图中夹持和加热装置去)

往试管A中加人研细的Cu(NO3)2 ·3H2O体并加热,观察到试管A中有红棕色气生成,最终残留黑色粉末;U型管中有液体生成,在试管B中收集到无色气体。
①当导管口不再有气池冒出时,反应停止,拆除装置的操作首先是______。
②试管B中收集到的气体一定含有______。
(4)锌与Cu(NO3)2溶液能发生反应。在一支试管中注人1 mol·L-1的Cu(NO3)2溶液,再放入一块锌片,观察到在反应初期有大量无色气泡冒出,同时锌片上析出红色固体。该小组猜想气体的成分,并设计的实验步骤,请填写下表。

查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市西城区高三上学期期末考试化学试卷(解析版) 题型:实验题
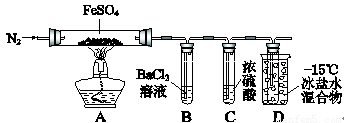
(8分)某小组取一定质量的FeSO4固体,利用下图装置进行实验。
|
|
实验过程 |
实验现象 |
|
① |
通入一段时间N2,加热 |
A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
|
② |
用带有火星的木条靠近装置D的导管口 |
木条复燃 |
|
③ |
充分反应,停止加热,冷却后,取A中固体,加盐酸 |
固体溶解,溶液呈黄色 |
|
④ |
将③所得溶液滴入D试管中 |
溶液变为浅绿色 |
已知:SO2熔点–72℃,沸点–10℃;SO3熔点16.8℃,沸点44.8℃。
(1)实验③反应的离子方程式是_______。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有______气体,依据是_______。
(3)实验④反应的离子方程式是_______。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,原因是(用必要的文字和化学方程式解释)_______。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省石家庄市高三补充题、压轴题化学试卷(解析版) 题型:选择题
已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用下图装置进行实验探究,下列说法正确的是()

A.X为锌棒,K置于M,可减缓铁的腐蚀,铁电极上发生的反应为2H++2e-=H2↑
B.X为锌棒,K置于M,外电路电流方向是从X到铁
C.X为碳棒,K置于N,可减缓铁的腐蚀,利用的是外加电流的阴极保护法
D.X为碳棒,K置于N,在X电极周围首先失电子的是Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com