
[选修 2—化学与技术]Ⅰ下列说法不正确的是
A.明矾、漂白粉、臭氧的净水原理相同
B.“血液透析”的原理利用了胶体的性质
C.食品包装中常放入有硅胶和铁粉的小袋,只能防止食物受潮
D.煤炭燃烧、机动车尾气、建筑扬尘等可加重雾霾
Ⅱ水是一种重要的自然资源,是人类赖以生存不可或缺的物质。 水质优劣直接影响人体健康。 海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。 据此,回答下列问题:
(1)天然水灾净化处理过程中需要加入的混凝剂,我们常用的混凝剂有明矾、硫酸铝、硫酸铁,其净水作用的原理是 。
(2)水的净化与软化的区别是水的净化是用混凝剂(如明矾等)将 。
(3)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。 蒸馏法是将海水变成蒸汽,蒸汽经冷却而得高纯度淡水。由此可判断蒸馏法是 (选填“物理变化”或“化学变化”)。
(4)海水除了可以得到淡化水外,还可提取多种化工原料。由海水制备无水氯化镁,主要有以下步骤:
①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④⑤③①
B.③②④①⑤
C.③④②⑤①
D.②④③⑤①
(5)海水电解制得的氢气用于合成氨,某合成氨厂生产流程图如下
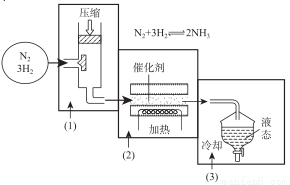
①第(1)个设备中先把N2和H2压缩的目的是 。
②在第(3)个设备中用冷却的方法分离出 ,其目的是 。
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源:2015-2016学年湖北省高二5月月考化学试卷(解析版) 题型:选择题
1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
CH2=CH-CH=CH2(g)+2H2(g) CH3CH2CH2CH3(g)
CH3CH2CH2CH3(g)  H=-236.3 kJ
H=-236.3 kJ mol-1
mol-1
CH3—C C—CH3(g)+2H2(g)
C—CH3(g)+2H2(g) CH3CH2CH2CH3(g)
CH3CH2CH2CH3(g)  H=-272.7 kJ
H=-272.7 kJ mol-1
mol-1
由此不能判断的是( )
A.1,3-丁二烯和2-丁炔稳定性的相对大小
B.1,3-丁二烯和2-丁炔分子储存能量的相对高低
C.1,3-丁二烯和2-丁炔相互转化的热效应
D.一个碳碳三键的键能与两个碳碳双键的键能之和的大小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:选择题
某多肽分子式为C46H71O24N13,完全水解后生成的产物为甘氨酸、丙氨酸、谷氨酸,则1mol该多肽彻底水解生成的谷氨酸(C5H9NO4)的物质的量为( )
A.3mol B.4mol C.5mol D.6mol
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨六中高三下三模理综化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质]A、B、C、D为原子序数依次增大的四种元素,A2-和B2+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的次外层电子排布式为 。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;B的氢化物所属的晶体类型是 ,B单质所形成的晶体,一个晶胞平均含有 个原子。
(3)C和D反应可生成组成比为1:5的化合物E,E的分子式为 ,已知该分子的空间构型为三角双锥,则其中两个Cl原子被F原子所替代得到的产物结构有 种。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与Na2SO3溶液反应,其离子方程式为 。
(5)A和B能够形成化合物F,F晶体中的B2+离子的排列方式如图所示,
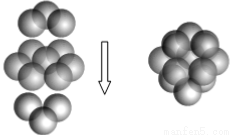
①每个B2+周围最近的等距离的B2+离子有 个。
②已知F的晶胞参数是a0=0.54nm,它的密度为 (只列式不作计算,阿伏加德罗常数为6.02×1023mol-1)。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨六中高三下三模理综化学试卷(解析版) 题型:选择题
水系锂电池具有安全、环保和价格低廉等优点,成为当前电池研究领域的热点。 以钒酸钠(NaV3O8)为正极材料的电极反应式为NaV3O8+xLi++xe-===NaLixV3O8,则下列说法不正确的是

A.放电时,负极的电极反应式:Li-e-===Li+
B.该电池可以用硫酸钠溶液作电解质
C.充电过程中阳极的电极反应式:NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化
D.充电过程中Li+从阳极向阴极迁移
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:填空题
焦炭与CO、CO2、H2均是重要的化工原料,由CO2制备甲醇过程可能涉及的反应如下:
反应Ⅰ:CO2 (g)+3H2 (g)  CH3OH(g)+H2O(g) △H1 =-49.58kJ·mol -1
CH3OH(g)+H2O(g) △H1 =-49.58kJ·mol -1
反应Ⅱ:CO2 (g)+H2 (g)  CO(g)+H2O(g) △H2 =+41.19kJ·mol -1
CO(g)+H2O(g) △H2 =+41.19kJ·mol -1
反应Ⅲ:CO(g)+2H2(g)  CH3OH(g) △H3
CH3OH(g) △H3
回答下列问题:
(1)反应Ⅲ的△H3 = ,反应Ⅲ自发进行的条件是 (填“较低温”、“较高温”或“任何温度”)。
(2)将焦炭与水蒸气置于容积为2L的密闭容器中发生反应:C(s) +H2O(g)  CO(g)+H2(g),其中H2O、
CO(g)+H2(g),其中H2O、
CO的物质的量随时间的变化曲线如图所示。

①0~1min 内用H2表示该反应的速率为 ,第一个平衡时段的平衡常数是 。
②若反应进行到2min时,改变了温度,使曲线发生如图所示的变化,则温度变化为 (填“升温”或“降温”)。
③反应至5min时,若也只改变了某—个条件,使曲线发生如图所示的变化,该条件可能是下述中的 。
a.加入了C(s) b.加入了水蒸气
c.降低了温度 d.增大了压强
(3)某研究小组将一定量的H2和CO2充入恒容密闭容器中并加入合适的催化剂(发生反应Ⅰ、Ⅱ、Ⅲ),测得了不同温度下体系达到平衡时CO2的转化率(曲线a)及CH3OH 的产率(曲线b),如图所示,请回答问题:
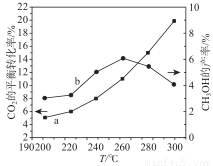
据图可知当温度高于260℃后,CO的浓度随着温度的升高而 (填“增大”、“减小”、“不变”或“无法判断”),其原因是 。
(4)若以CO、O2、K2CO3等构成的熔融盐电池为电源,用惰性电极电解200mL 饱和食盐水,则负极上的电极反应式为 ,当有2.8g燃料被消耗时,电解池中溶液的pH= (常温下,忽略溶液的体积变化,不考虑能量的其他损耗)。
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:选择题
取一定质量含Cu、Cu2O、CuO的固体混合物,将其分成两等份并进行下列转化,则转化过程中所加稀HNO3的物质的量浓度为
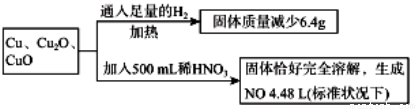
A.4.4mol·L -1 B.3.6mol·L -1 C.4.0mol·L -1 D.3.2mol·L -1
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:选择题
往碘化亚铁溶液中缓慢通入1.5mol氯气,反应完成后溶液中有1/2的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量为
A.1.1mol B.1.5mol C.1.2mol D.1.0mol
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三第八次月考理综化学试卷(解析版) 题型:选择题
下列有关电解质溶液的说法,不正确的是
A.pH 相同的NH4Cl,(NH4)2SO4溶液: c(NH4Cl) >c[(NH4)2SO4]
B.少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大
C.等物质的量浓度的HA与NaA溶液等体积混合后,混合溶液一定呈酸性
D.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)=c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com