
| A. | 电解质溶液导电的过程实际上就是电解的过程 | |
| B. | 利用电解饱和食盐水所得的产物可以生产盐酸 | |
| C. | 氢氧燃料电池的负极通入的是氢气 | |
| D. | 铜在酸性环境中易发生析氢腐蚀 |
分析 A.电解质溶液导电是阴阳离子在电极上发生的氧化还原反应,发生了电解;
B.电解饱和食盐水可得到氢气、氯气;
C.负极发生氧化反应;
D.铜与氢离子不反应.
解答 解:A.电解质溶液导电是阴阳离子在电极上发生的氧化还原反应,电解质溶液的导电过程就是电解的过程,故A正确;
B.电解饱和食盐水可得到氢气、氯气,二者反应可生成氯化氢,可用于制备盐酸,故B正确;
C.氢氧燃料电池的负极发生氧化反应,氢气被氧化生成水,负极应通入的是氢气,故C正确;
D.铜不能被氢离子氧化,铜发生吸氧腐蚀,故D错误.
故选D.
点评 本题考查了电化学方面的知识,涉及电解池和原电池原理,侧重于化学与生活的考查,有利于培养学生良好的科学素养,难度不大,要注重对基础知识的积累和运用.


科目:高中化学 来源: 题型:解答题
| 序号 | 实验步骤 | 肯定不存在的离子 |
| ① | 用pH试纸测得该溶液呈酸性 | |
| ② | 另取10mL该溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,在整个滴加过程中无沉淀生成 | |
| ③ | 往②所得溶液中加入足量Na2CO3溶液,过滤、洗涤、干燥,得到1.97g白色固体 | |
| ④ | 另取10mL该溶液,加入浓NaOH溶液并加热,收集到224mL,气体(标准状况) | |
| ⑤ | 另取10mL该溶液,加入足量稀HNO3和AgNO3,产生2.87g白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入苯或四氯化碳操作叫萃取 | B. | 苯层在下层或四氯化碳在上层 | ||
| C. | 可以用酒精代替苯或四氯化碳 | D. | 氯水是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸与氢氧化钡溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| B. | 硫酸铝溶液中滴入氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | 铜粉加入FeCl3溶液:Cu+Fe3+=Cu2++Fe2+ | |
| D. | 硝酸铝溶液中滴加少量的氢氧化钠溶液:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
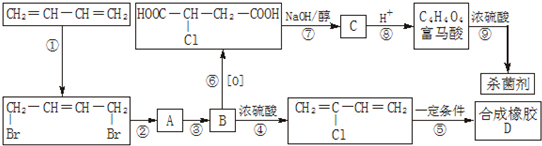
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com