
| A. | 若A遇NaHCO3溶液有气体生成,则A的结构共有4种 | |
| B. | 若A遇稀硫酸能生成两种有机物,则A的结构共有4种 | |
| C. | 若A能发生银镜反应,则A的结构有2种 | |
| D. | 若A既能和新制Cu(OH)2反应产生砖红色沉淀,又能和金属钠反应放出H2,则A的结构有3种 |
分析 A、遇NaHCO3溶液有气体生成,那么C4H8O2属于羧酸类,为饱和一元羧酸;
B、遇稀硫酸生成两种产物,说明为酯类;
C、能发生银镜反应,则应为甲酸某酯或羟基醛,据此判断即可;
D、C4H8O2属于羟基醛时,可以根据官能团的位置异构得到其同分异构体.
解答 解:A、C4H8O2属于羧酸时,是丁酸、2-甲基丙酸,共两种同分异构体,故A错误;
B、C4H8O2属于酯类的同分异构体,为饱和一元酯,为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇可以可知1个-OH取代丙烷中的H原子,丙烷分子中有2种H原子,形成的丙醇有2种,形成的酯有2种,为乙酸与乙醇形成的酯,只有乙酸乙酯1种,为丙酸与甲醇形成的酯,注意丙酸甲酯1种,故C4H8O2属于酯类的同分异构体共有4种,故B正确;
C、分子式为C4H8O2能发生银镜反应,说明含有醛基,则可能为甲酸丙酯,甲酸有1种,丙醇有2种,甲酸丙酯共2种;
可能为羟基醛,丁醛有2种,羟基丁醛有5种:CH2OHCH2CH2CHO、CH3CH2OHCH2CHO、CH3CH2CH2OHCHO,CH2OHCHCH3CHO、(CH3)2CHCHO;
可能为醚醛,醚醛有3种:CH3CH2CH2OCHO、CH3CH2OCH2CHO、CH3OCH2CH2CHO;所以共有10种,故C错误;
D、C4H8O2属于羟基醛时,可以是2-羟基丁醛、3-羟基丁醛、4-羟基丁醛、2-甲基-2-羟基丙醛、2-甲基-3羟基丙醛,共5种同分异构体,故D错误;故选B.
点评 本题考查酯类同分异构体的判断,是高考中的常见题型,属于中等难度的试题,试题基础性强,侧重对酯类组成与结构的熟悉掌握程度,有利于培养学生的逻辑推理能力.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
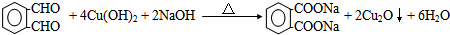
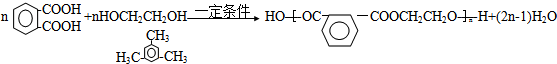
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
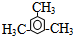
| A. | 草酸二苯酯的分子式是C14H10O4 | |
| B. | 上述变化证明化学能可以转化为光能 | |
| C. | C2O4的结构简式 | |
| D. | 反应①属于酯水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 己知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的最外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应也能与NaOH溶液反应.元素Q是地壳中含量第二位的金属元素.试回答下列问题:
己知X、Y、Z、W为短周期四种常见元素,其中X是原子半径最小的元素,Y原子的最外层电子数是内层电子数二倍,Z能和X形成两种常见的液态化合物,W元素的单质既能与盐酸反应也能与NaOH溶液反应.元素Q是地壳中含量第二位的金属元素.试回答下列问题: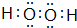 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8g重水中含有的电子数为NA | |
| B. | 1L0.1mol/L FeCl3溶液中含有的Cl- 数为0.3NA | |
| C. | 25℃,1L pH=13的Ba(OH)2溶液中含有的oH-数为0.2NA | |
| D. | 标准状况下,2.24L NO和NO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池要进入广泛的实际应用,高容量储氢材料的研制是需解决的关键技术问题之一 | |
| B. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| C. | 2013年6月航天员王亚平在太空做的水膜实验说明:水分子的组成和结构在太空中发生了改变,水才有不同于其在地球上的物理现象 | |
| D. | 元素分析仪可检验C、H、O、N、S等非金属元素,也可以检验Cr、Mn等金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 某溶液100mL,其中含硫酸0.03mol,硝酸0.04mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015mol | |
| B. | 室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧.则a、b的关系是a=4b+c | |
| C. | 已知某温度Ksp(Ag2S)=6×10-50,Ksp(AgCl)=2×10-6,则2AgCl(s)+S2-(aq)?Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×10-37 | |
| D. | 在25℃下,将2a mol•L-1的氨水与0.02 mol•L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),则用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{10-9}{a-0.01}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com