
��16�֣������ƾ���(Na2MoO4��2H2O)����������ȴˮϵͳ�Ľ�����ʴ�������⾫����Ҫ�� ����MoS2��������PbS�ȣ��Ʊ������ƾ���IJ����������£�
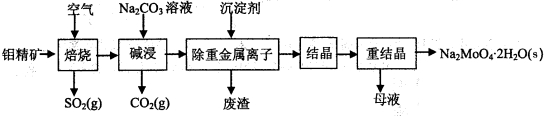
��1�����յĹ����в��õ��ǡ��������ա��Ĵ�ʩ����ô�ʩ���ŵ��ǣ� ��
��2��д������ʱ����MoO3�Ļ�ѧ����ʽΪ�� ��
��3��д�����������Ӧ�����ӷ���ʽ�� ��
��4�����Һ�ᾧǰ�����Ba(OH)2�����Գ�ȥSO42������BaMoO4��ʼ����ʱ����SO42����ȥ���ʣ�д��������̣�����֪�����Һ��c(MoO42��)=0.40mol��L��1��c(SO42��)=0.040mol��L��1��Ksp(BaSO4)= 1.0��10��10��Ksp(BaMoO4)= 4.0��10��8������Ba(OH)2�����������Һ����仯�ɺ��ԡ�
��5����ͼ��̼����3�ֲ�ͬ�����еĸ�ʴ����ʵ������
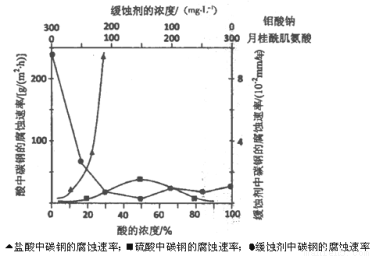
��̼��������������и�ʴ���������Ũ�ȱ仯�����Բ��죬��ԭ������� ��
�ڿ����������ζ�̼�ֵĻ�ʴԭ�����ڸ��������γ�FeMoO4~Fe2O3����Ĥ���ܱ�ʽѭ����ȴˮϵͳ�е�̼�ֹܵ���ʴ���������������������NaNO2����NaNO2������ ��
 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡӥ̶�и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ɫϡ��ҺX�У����ܺ����±����������е�ij����
������ | CO32-��SiO32-��AlO2-��Cl- |
������ | Al3+��Fe3+��Mg2+��NH4+��Na+ |
��ȡ����Һ�����������м���ij�Լ�Y���������������ʵ�����n��������Լ�Y�����V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
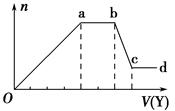
A����Y�����ᣬ��Oa��ת��Ϊ���������ӣ��ϱ��У���ͬ��ֻ��AlO2-
B����Y�����ᣬ����Һ�п��ܺ��е���������Al3+��
C����Y��NaOH��Һ����bc�η�Ӧ�����ӷ���ʽΪ Al��OH��3+OH-=AlO2-+2H2O
D����Y��NaOH��Һ����X��Һ��ֻ�����������ǣ�Al3+��Fe3+ ��NH4+ ��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и���ѧҵˮƽģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�鷽���ܴﵽʵ��Ŀ�ĵ���
A���õ�����Һ������Һ���Ƿ���ڵⵥ��
B���÷�Һ©������ˮ���Ҵ��Ļ����
C�����Ȼ�����Һ����̼������Һ����������Һ
D������ˮ�������ռ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡտ���и�����ͨ�߿����ԣ��������ۻ�ѧ�Ծ��������棩 ���ͣ������
��16�֣�ij��ҵ�ϲ�����ĩ��SiO2��Fe2O3��CeO2��FeO�ȡ�ij����С��������¹������̶���Դ���л��գ��õ�Ce(OH)4��������立���
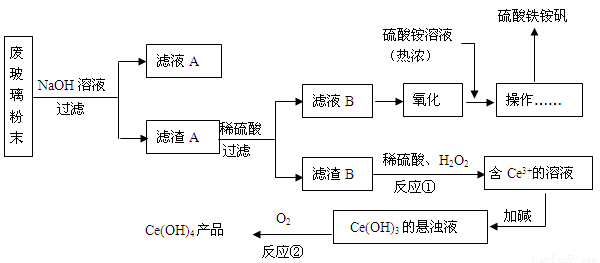
��֪��CeO2������ϡ������������£�Ce3+��ˮ�⣬Ce4+�н�ǿ�����ԡ�
��1��������立��ɾ�ˮ����ԭ���ǣ�д���ӷ���ʽ�� ��
��2����ҺA����Ҫ�ɷ� ����д��ѧʽ����
��3����Ӧ�ٵ����ӷ���ʽ�� ��
��4����Ӧ�ڵĻ�ѧ��Ӧ����ʽ�� ��
��5����֪��������立������Fe2(SO4) 3��(NH4) 2SO4��24H2O��ʽ��964�ݵIJ���Ϊ80%��������13.2g (NH4) 2SO4��ʽ��132�������Ƶþ���������� ��
��6��������HT����Ϊ��ȡ���ܽ������Ӵ�ˮ��Һ����ȡ���������̱�ʾΪ��
Ce2(SO4)3 (ˮ��)+ 6HT(�л���) 2CeT3 (�л��㣩+3H2SO4(ˮ��)
2CeT3 (�л��㣩+3H2SO4(ˮ��)
��Һ�õ�CeT3 (�л��㣩���ټ���H2SO4 ��ýϴ��ĺ�Ce3+��ˮ��Һ����ѡ������������ȡ����ԭ���� ����ƽ���ƶ��ǶȻش𣩡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡտ���и�����ͨ�߿����ԣ��������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���г�������ȷ�����������ϵ����
ѡ�� | ������ | ������ |
A | SO3����ˮ���ܵ��� | SO3Ϊ����� |
B | ����ͭ���� | ͭ���ϵ������ڳ�ʪ�������������� |
C | ŨH2SO4��ǿ������ | ŨH2SO4����������Cu������Ӧ |
D | С�մ�������Ƹ������ɼ� | NaHCO3����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ�����и�����ҵ���ģ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼΪEFC���ŷ��ù����������(TiO2)���������ѵ�װ��ʾ��ͼ����ԭ�����ڽϵ͵�������λ�£�TiO2(����)�е���������������Σ��������ֻʣ�´��ѡ�����˵������ȷ����

A�������ĵ缫��ӦʽΪ��2Cl����2e��= Cl2��
B��ͨ���O2����Cl�����������ƶ�
C�������ĵ缫��ӦʽΪTiO2+4e��=Ti+2O2��
D��ʯī�缫�������������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫�߿���ɽ�и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
����������Ҫ�ɷ���TiO2������FeO��Fe2O3���Ʊ�TiCl4���̷��Ȳ�Ʒ��һ���ۺϹ�������ͼ���£�
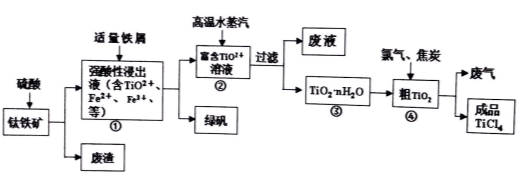
����ʾ��TiO2+��ˮ��ƽ��TiO2++��n+1��H2O TiO2��n H2O+2H+
TiO2��n H2O+2H+
�ش��������⣺
��1��������������ѷ�Ӧ�����ӷ���ʽ�� ��
��2����֪��TiO2��s��+2Cl2(g��=TiCl4(l��+O2(g�� ��H = +140 kJ��mol��1
2C(s��+ O2(g��=2CO(g�� ��H = -221 kJ��mol��1
д������TiO2�ͽ�̿��������Ӧ����Һ̬TiCl4 ��CO������Ȼ�ѧ����ʽ�� ��
��3�������м�����м������Һ����ɫ����ʱ��Һ�Գ�ǿ���ԡ��ù����������·�Ӧ������
A��2Fe3++Fe=3Fe2+
B��2 TiO2+(��ɫ�� +Fe+4H+��2Ti3+(��ɫ��+ Fe2++2H2O
C��Ti3+(��ɫ��+ Fe3++H2O��TiO2+(��ɫ�� +Fe2++2H+
I�������Ϣ�ж�Fe3+ ��TiO2+�� H+������ǿ���� > >
II��������������� ��
��4�������в���ͨ�����ˮ������ά����Һ����һ��ʱ�䣬����ˮ�϶������ѳ�����
���û�ѧƽ�����۷���ͨ�����ˮ���������ã� ��
��5��������ɫ��ѧ����ù��������д��ڵIJ���֮���� ��ֻҪ��д��һ���
��6���̷���Ħ������Ϊ278g/mol��������������ɫ���ϣ�Fe2O3����556akg�̷��������Ͽ�������ɫ����___mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�ɶ��и���4��ģ�⿼���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���к�MgCl2��AlCl3��Ϊn mol�Ļ����Һ,�����е�NaOH��Һ������������NaOH��Һ�����ʵ��������ɳ��������ʵ����Ĺ�ϵ��ȷ����(�����γɳ�����������ܽ�����ҺpH�Ĺ�ϵ���±�)
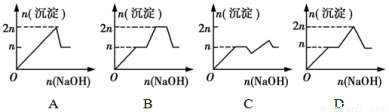
���� | Mg2+ | Al 3+ | ���� | Al(OH)3 |
��ʼ����ʱ��pH | 8.93 | 3.56 | ��ʼ�ܽ�ʱ��pH | 8.04 |
��ȫ����ʱ��pH | 10.92 | 4.89 | ��ȫ�ܽ�ʱ��pH | 12.04 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������и������¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣�ʵ���������᳧��������Ҫ�ɷ�ΪFe2O3������FeS��SiO2�ȣ��Ʊ���������ʽ�������ľۺ����Fe(OH)(SO4)��n���̷�(FeSO4��7H2O)���������£�
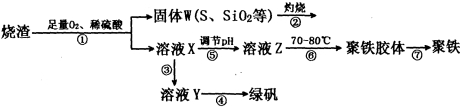
��1���ڢ�����֪FeS����Ԫ������Fe3+��SԪ�����ɵ�����д��FeS��O2��H2SO4��Ӧ�����ӷ���ʽ______________________________________��
��2�������̢��в���������ͨ��������Һ�У���Һ������ɫ����___________�����ţ���
A��Ʒ����Һ B������KMnO4��Һ
C����ɫʯ����Һ D����ˮ
��3���ڢ��У�������������___________________________��
��4���ڢ��У�����Ũ����Ҫ�Ĺ������������ƾ����⣬����___________________________��
��5���ڢ��У�����ҺZ���Ƶ�70��80���Ŀ����____________________________________��
��6��Ϊ����������Ʒ����Ԫ�ص�������������������ʵ�飨���������в�����Ԫ�غ���Ԫ�أ�����ȡһ��������Ʒ������Ʒ����������_________���ѧʽ����ͬ�����μӹ�����__________��������������ij��������ˡ�ϴ�ӡ�����������������������þ�����Ʒ����Ԫ�ص�����������
��7�����ò���ۢ���ȡ�̷����ⶨ3g����������������������
��ȡ�����̷���Ʒ���ܽ⣬���Ƴ�1000mL��Һ����ȡ25.00mL������Һ����ƿ�У�������Һʱ��Ҫ�IJ�������������������Ͳ���ձ�����ͷ�ι��⣬���� ��
���������ữ��0.01000mol/L KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ15.00mL���жϴ˵ζ�ʵ��ﵽ�յ�ķ����� �����ڵζ��յ��ȡ�ζ��̶ܿ�ʱ������KMnO4��ҺҺ�棬������������ȷ����ʹ�ⶨ��� ���ƫ�ߡ���ƫ�͡�����Ӱ�족����
�ۼ�����������Ԫ�ص���������Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com