
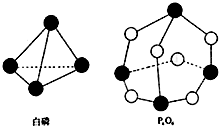
 ��ѧ��Ӧ�ı����Ǿɽ��Ķ��Ѻ��¼����γɹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ•mol-1��P-P��198 P-O��360 O=O��498����ӦP4�����ף�+3O2��P4O6�������仯Ϊ��������
��ѧ��Ӧ�ı����Ǿɽ��Ķ��Ѻ��¼����γɹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ•mol-1��P-P��198 P-O��360 O=O��498����ӦP4�����ף�+3O2��P4O6�������仯Ϊ��������| A�� | ����126kJ������ | B�� | �ͷ�126kJ������ | ||
| C�� | ����1638kJ������ | D�� | �ͷ�1638kJ������ |
���� ��Ӧ�ȡ�H=��Ӧ���ܼ���-�������ܼ��ܣ��ݴ˼����жϣ�ע��ÿĦ��P4�к���6molP-P����
��� �⣺����ѧ������ΪP-P 198kJ•mol-1��P-O 360kJ•mol-1��O=O 498 kJ•mol-1��
��Ӧ�ȡ�H=��Ӧ���ܼ���-�������ܼ��ܣ�
���Է�ӦP4+3O2=P4O6�ķ�Ӧ�ȡ�H=6��198kJ•mol-1+3��498kJ•mol-1-12��360kJ•mol-1=-1638kJ•mol-1��
��ѡD��
���� ���鷴Ӧ���뻯ѧ�����ܵĹ�ϵ���Ѷ��еȣ�ע��������������������ⷴӦ�ȣ�


 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԭ�ӽṹʾ��ͼ��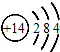 | |
| B�� | ԭ�Ӻ�����8�����ӵ���ԭ�ӣ�${\;}_{8}^{18}$O | |
| C�� | ������̼���ӵĵ���ʽ��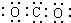 | |
| D�� | ������ӵı���ģ�ͣ�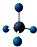 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ܢ� | B�� | �ڢۢ� | C�� | �٢ۢܢ� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
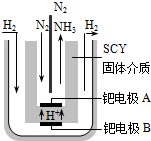 �ϳɰ���ҵ�����Ṥҵ�Թ���ũ��������������Ҫ���壮��ش�
�ϳɰ���ҵ�����Ṥҵ�Թ���ũ��������������Ҫ���壮��ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
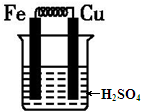
| A�� | ���缫Ϊ������ͭ�缫Ϊ���� | B�� | �����е�������Ϊ����ͭ | ||
| C�� | ��Һ���������������缫 | D�� | �����缫��Ӧʽ��2H++2e-�TH2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ198 | B�� | ������Ϊ140 | C�� | ������Ϊ82 | D�� | ���������Ϊ58 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���������� | ���� | |
| A | ����С��ͬ��K��Na����������ˮ�У��ر��Ʒ�Ӧ���� | ��Ԫ�صĽ����Ա���Ԫ��ǿ |
| B | ��Ba��OH��2•8H2O��NH4Cl������С�ձ��л�ϣ����ִ����ձ���ڸо����� | Ba��OH��2•8H2O��NH4Cl�ķ�Ӧ�����ȷ�Ӧ |
| C | ��ʢ��H2O2��Һ���Թ��У���������FeCl3��Һ���������ݵ����ʱȲ���FeCl3��Һ�Ŀ� | FeCl3���Լӿ�H2O2�ֽ�����ʣ����˴����� |
| D | ������KMnO4��Һ��ͨ��SO2���壬KMnO4��Һ��ɫ��ȥ�� | SO2����Ư���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ��H=-890.3kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ•mol-1 | |
| B�� | ��֪H2O��l���TH2O��g����H=+44 kJ•mol-1����2gH2��g����ȫȼ������Һ̬ˮ��������̬ˮ���ͷ�22kJ������ | |
| C�� | ���ȷ�Ӧһ���Ƿ��Է��Ļ�ѧ��Ӧ | |
| D�� | ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com