
【题目】分别取V L含有Na2SO4和Al2(SO4)3的混合溶液两等份,一份加入含a mol NaOH的溶液,恰好使Al3+完全转化为AlO2-;另一份加入含b mol BaCl2的溶液,恰好使SO42-完全沉淀为BaSO4。则原混合溶液中Na+的浓度为 ( )
A. 8b-3a/2V molL-1 B. 8b-3a/4V molL-1
C. a-2b/V molL-1 D. a-2b/2V molL-1
【答案】A
【解析】混合溶液分成两等份,每份溶液浓度相同.一份加入含a mol NaOH的溶液,恰好使铝离子完全转化为AlO2-,根据四羟基合铝酸根离子化学式,可知该份中n(Al3+)=n(AlO2-)=![]() n(NaOH)=
n(NaOH)=![]() amol;另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4,根据钡离子与硫酸根守恒可知该份中n(SO42-)=BaSO4=n(BaCl2)=bmol;由电荷守恒可知每份中n(Na+)+3n(Al3+)=2(SO42-),即n(Na+)+3×
amol;另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4,根据钡离子与硫酸根守恒可知该份中n(SO42-)=BaSO4=n(BaCl2)=bmol;由电荷守恒可知每份中n(Na+)+3n(Al3+)=2(SO42-),即n(Na+)+3×![]() amol=2×bmol,解得n(Na+)=(2b-
amol=2×bmol,解得n(Na+)=(2b-![]() a)mol,所以原混合溶液中Na+的浓度为
a)mol,所以原混合溶液中Na+的浓度为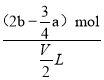 =
=![]() mol/L。答案选A。
mol/L。答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一:焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2![]() Na2S2O5。
Na2S2O5。

(1)加试剂前要进行的操作是_______________。装置Ⅰ中产生气体的化学方程式为____________。
(2)浓硫酸_______________ (填“能”或“不能”)用稀硫酸代替,原因是_______________。
(3)从装置Ⅱ中分离出产品可采取的分离方法是_______________________。
(4)为了完整实验装置,在下列装置中选择一个最合理的装置放在装置Ⅲ处,可选用的装置(夹持仪器已略去)为___________(填序号)。

实验二:葡萄酒中抗氧化剂残留量的测定
(5)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O![]() H2SO4+2HI)
H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液30.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果______________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. NaAlO2溶液中通入过量的CO2:2AlO![]() +3H2O+CO2===2Al(OH)3↓+CO
+3H2O+CO2===2Al(OH)3↓+CO![]()
B. 明矾溶液中滴加Ba(OH)2溶液至SO![]() 完全沉淀:Al3++Ba2++SO
完全沉淀:Al3++Ba2++SO![]() +3OH-===BaSO4↓+Al(OH)3↓
+3OH-===BaSO4↓+Al(OH)3↓
C. 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br-+5Cl2===4Fe3++3Br2+10Cl-
D. 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3===2FeO![]() +3Cl-+H2O+4H+
+3Cl-+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是
A. CS2是V形分子 B. SnBr2键角大于120°
C. BF3是三角锥形分子 D. NH4+键角等于109.5°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某样品中含有碳酸钠及少量的硫酸钠和氯化钠,某学生为检验其中的阴离子,按照下图程序进行实验,所加试剂均过量。(可供选择的试剂有:稀硫酸、稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液)

回答下列问题:
(1)①试剂1是________结论1是________;
②试剂2是________结论2是________;
③试剂3是________结论3是________ 。
(2)写出有关反应的离子方程式
①__________________;
②__________________;
③__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列加横线的字所指代物质的主要成分与其他三项不同的是( )
A.儿童散学归来早,忙趁东风放纸鸢B.黑发不知勤学早,白首方悔读书迟
C.散入珠帘湿罗幕,狐裘不暖锦衾薄D.绚丽丝绸云涌动,霓裳歌舞美仙姿
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是

A.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
B.C点的沉淀为Fe(OH)3
C.OA段可能发生的反应是:3Ba2++6OH-+3SO42-+Fe3++Al3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.据图计算原溶液中c(Cl-)>c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2是一种主要的大气污染物。下列关于NO2性质的描述不正确的是 ( )
A. 无色 B. 易溶于水 C. 有刺激性气味 D. 密度比空气的大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com