
 2 Z(g),达到平衡时,若它们的物质的量满足:n(X)+n(Y)= n(Z),则Y的转化率为
2 Z(g),达到平衡时,若它们的物质的量满足:n(X)+n(Y)= n(Z),则Y的转化率为
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.在平衡常数表达式中,反应物的浓度为初始浓度,生成物的浓度为平衡浓度 |
| B.在任何条件下,化学平衡常数都是一个恒定值 |
| C.平衡常数的大小只与浓度有关,与温度、压强、催化剂等无关 |
| D.从平衡常数的大小可以判断一个反应进行的程度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.恒温、恒压时,充入NH3 | B.恒温、恒容时,充入N2 |
| C.恒温、恒压时,充入He | D.恒温、恒容时,充入He |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO2+H2(g) 反应过程中测定的部分数据见下表(表中t2>t1):
CO2+H2(g) 反应过程中测定的部分数据见下表(表中t2>t1):| 反应时间/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2H2+O2、2CO+O2
2H2+O2、2CO+O2 2CO2
2CO2查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g) +H2(g) △H= +131.3kJ·mol-1
CO(g) +H2(g) △H= +131.3kJ·mol-1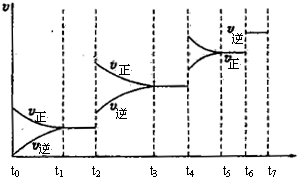
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Z(g),经60s达到平衡,生成0.15molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.15molZ。下列说法正确的是| A.将容器体积变为10L,Z的平衡浓度变为原来的二分之一 |
| B.以Y浓度变化表示的反应速率为0.0005mol /(L· s) |
| C.若增大压强,则物质Y的转化率减小 |
| D.若降低温度,X的体积分数增大,则该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


 常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH值调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)
常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH值调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) △H<0,673K、30MPa下n(NH3)和n(H2)随时间变化的关系
2NH3(g) △H<0,673K、30MPa下n(NH3)和n(H2)随时间变化的关系 如下图所示。下列叙述不正确的是
如下图所示。下列叙述不正确的是
| A.点a的正反应速率比点b的大 |
| B.点c处反应达到平衡 |
| C.点d (t1时刻) 和点e (t2时刻) 处n(N2)一样多 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com