
����Ŀ����֪����R��Br�D��R��OH(R��ʾ����)��
�ڱ�����ԭ�е�ȡ�������µ����ȡ�������뱽����λ����������Ӱ�죻
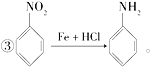
�������ñ���Ϊԭ���Ʊ�һϵ�л������ת����ϵͼ��
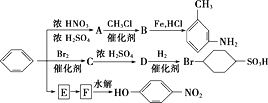
(1)д��Aת��ΪB�Ļ�ѧ����ʽ��______________________��
(2)ͼ�б�ת��ΪE��Eת��ΪFʡ������������д��E��F�Ľṹ��ʽ��
E________________��F_____________________��
(3)B�����б����ϵ����������ⱻ��ԭ��ȡ���õ��Ķ��������____��ͬ���칹�塣
(4)����ת�����漰��9����Ӧ�����в�����ȡ����Ӧ�Ĺ���_____����
���𰸡�
![]()
![]() 62
62
��������
��1����B����������ԭ���������֪Aת��ΪBʱ����ļ��������ļ�λ���ʴ�Ϊ��![]() ����2����������-��A-��B��������-��C-��D����2��ת�������ɵ�һ��ת������֪������������������-CH3����-CH3��-NO2�ļ�λ���ɵڶ���ת������֪������±���ٻǻ�����-SO3H��-Br�Ķ�λ����Fˮ��õ�
����2����������-��A-��B��������-��C-��D����2��ת�������ɵ�һ��ת������֪������������������-CH3����-CH3��-NO2�ļ�λ���ɵڶ���ת������֪������±���ٻǻ�����-SO3H��-Br�Ķ�λ����Fˮ��õ�![]() ��˵��F��-Cl����-Br��λ��-NO2�Ķ�λ������-��E-��F��Ӧ����±������������E��
��˵��F��-Cl����-Br��λ��-NO2�Ķ�λ������-��E-��F��Ӧ����±������������E��![]() ��������
��������![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��![]() ����3��B�ĽṹΪ��
����3��B�ĽṹΪ��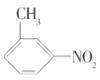 �����ӽṹ�Dz��ԳƵģ�������ʣ���ĸ���ԭ�Ӷ��Dz���Ч�ģ�������������������ԭ��ȡ���ɵõ�һ�ֲ�ͬ�Ķ�����ͨ���������
�����ӽṹ�Dz��ԳƵģ�������ʣ���ĸ���ԭ�Ӷ��Dz���Ч�ģ�������������������ԭ��ȡ���ɵõ�һ�ֲ�ͬ�Ķ�����ͨ���������![]() =6�ɵ���6�֣������ľŸ���Ӧ�еķ�Ӧ�����漰��ȡ����Ӧ���ӳɷ�Ӧ�ͻ�ԭ��Ӧ���ʴ�Ϊ��6��2��
=6�ɵ���6�֣������ľŸ���Ӧ�еķ�Ӧ�����漰��ȡ����Ӧ���ӳɷ�Ӧ�ͻ�ԭ��Ӧ���ʴ�Ϊ��6��2��


 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д� �ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
�ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ����ȷ����(����)
A. �����ȼ������H����890.3 kJ��mol��1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ CH4(g)��2O2(g)===CO2(g)��2H2O(g)����H����890.3 kJ��mol��1
B. 500 �桢30 MPa������0.5 mol N2(g)��1.5 mol H2(g)�����ܱ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪN2(g)��3H2(g)![]() 2NH3(g)����H����38.6 kJ��mol��1
2NH3(g)����H����38.6 kJ��mol��1
C. HCl��NaOH��Ӧ���к�����H����57.3 kJ��mol��1����H2SO4��Ca(OH)2��Ӧ���к�����H��2��(��57.3)kJ��mol��1
D. ��101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ2H2(g)��O2(g)===2H2O(l)����H����571.6 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC5H12O �Ĵ���ͬ���칹�����ĿΪ�������������칹��( )
A.3��B.4 ��C.5 ��D.6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Ϣ������л�ѧʵ�����⣺
����ȩ������Ҫ�Ĺ�ҵԭ�ϣ����Ը����������Ʊ�����Һ��Ӧ���������������ǻ������ƣ�������ˮ�������ڱ���������������Һ��R-CHO+NaHSO3![]() R-CH��OH)-SO3Na
R-CH��OH)-SO3Na
��1��������Ӧ����Ϊ________��Ӧ����ʹCH3 CH��OH)-SO3Naȫ�������ȩ���ɲ��õ��Լ���__________��__________��������ȩ�IJ������� _____________��
������ʵ�������ñ���ȩ����Ϣ��ȩ���Ʊ����״��ͱ�����Ļ�ѧԭ����
![]() ����ԭ������������-���ȩ��
����ԭ������������-���ȩ��
��֪�������ʵ����ʣ�
���״����۵�(��):-15.3�棬������ˮ���������л��ܼ���
����ȩ���۵�(��):-26�棬����ˮ���������л��ܼ���
������ܽ��Ϊ0.344g��25�������������л��ܼ�����Ҫ������ͼ��ʾ��
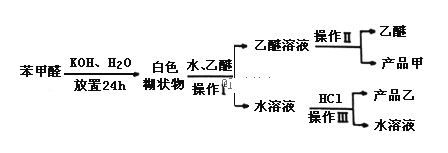
�ش��������⣺
��2����������������___________��������Һ�����ܽ����Ҫ�ɷ���__________��
��3����������������________����Ʒ����_______________��
��4���������������õIJ�Ʒ���г�����һ�������л�����___________����д���ʵ����ƣ������������Լ�������KMnO4��ϡNaOH��Һ��ϡH2SO4������NaHSO3��Һ��д�������Ʒ���к��и����ʵĹ��̣�______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2011��12�½���ͭҵ���ۻ������Σ��ݲⶨ��ˮ���ؽ�����Ⱦ����ж��ǽ�����Ⱦ����ʮ���֣����������ؽ����ж���֢������ֲ�ʱ�з����� ��ˮ�е��ؽ���ָ���ǣ� ��
A. �������� B. ����Ԫ�� C. ����ͭ D. ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij100mL��Һ���ܺ���Na+��NH4+��Fe3+��CO32-��SO42-��Cl-�е������֣�ȡ����Һ��������ʵ�飬ʵ��������£��������Լ�������������ȫ���ݳ���
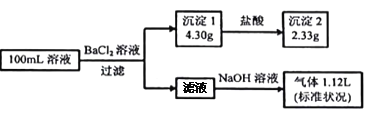
����˵������ȷ����
A. ԭ��Һһ������CO32-��SO42-��һ��������Fe3+
B. ��ԭ��Һ�в�����Na+����c(Cl-)��0.1mol��L-1
C. ԭ��Һ��c(Cl-)��0.1mol��L-1
D. ԭ��Һһ������Cl-�����ܴ���Na+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ˮ��ɹ�ɵô��Σ����γ�NaCl�⣬������MgCl2��CaCl2��Na2SO4�Լ���ɳ�����ʡ��������Ʊ����ε�ʵ�鷽�������������������£�
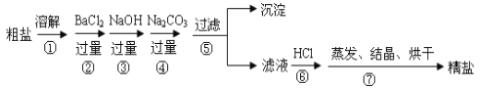
��1���ڵڢٲ������ܽ������Ҫ�ò��������裬������___________________________��
��2���ڢڲ�������Ŀ���dz�ȥ�����е�__________���ѧʽ�����ж�BaCl2�ѹ����ķ�����____________________________________________________________��
��3���ڵڢ۲������У�ѡ��ij��ӵ��Լ�������KOH����NaOH��������________________��
��4���ڢݲ��������������еõ������ijɷ��У���ɳ��BaSO4��________��__________��
��5���������ᾧ���õ��������У�����̨(��Ȧ)������ǯ���ƾ��ơ����������______��
��6���ڢܲ���ԭʳ��������������̼����ķ�Ӧ��еķ�Ӧ�����ӷ���ʽΪ��______________________________��
��7���ڢ��������漰��Ӧ�����ӷ���ʽ�У�__________________��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ���ڱ��ж����ڵ�һ���֡���֪aԭ�ӵ�������ϵĵ�����Ŀ�Ǵ���������Ŀ��һ�룬����˵���в���ȷ����( )

A. Ԫ��a������������ˮ��������Ա�b��
B. Ԫ��a��ԭ�Ӱ뾶��d�Ĵ�
C. Ԫ��a�ĵ����ڿ�����ȼ�ջᵼ��������ЧӦ��
D. Ԫ��a������һ�����õİ뵼�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�кܶ���Ҫ��ԭ�϶�����Դ��ʯ�ͻ������ش��������⡣
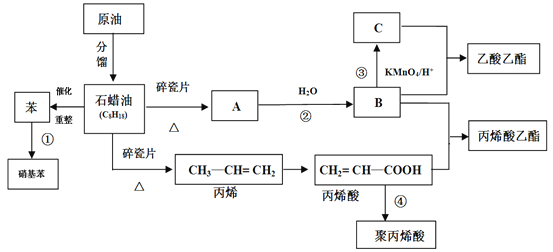
(1)A���ṹ��ʽΪ________��
(2)��ϩ�������������ŵ�����Ϊ_______��
(3)�٢۷�Ӧ�ķ�Ӧ���ͷֱ�_______��_______��
(4)д�����з�Ӧ����ʽ
�ٷ�Ӧ�ڵķ���ʽ_____________________��
�ڷ�Ӧ�ܵķ���ʽ_____________________��
�۱�ϩ��+B����ϩ������________________��
(5)��ϩ��(CH2=CH��COOH)�����ʿ�����_______
�ټӳɷ�Ӧ ��ȡ����Ӧ �ۼӾ۷�Ӧ ���кͷ�Ӧ ��������Ӧ
A��ֻ�Т٢� B��ֻ�Т٢ۢ�
C��ֻ�Т٢ۢܢ� D���٢ڢۢܢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com