
 NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,反应的化学方程式为2CO+2NO?N2+2CO2△H<0
NO和CO都是汽车尾气中的有害物质,它们能缓慢地起反应,反应的化学方程式为2CO+2NO?N2+2CO2△H<0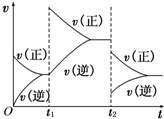 ,
, .
.


科目:高中化学 来源: 题型:
| A、在食盐中加适量乳酸锌以防止儿童缺锌 |
| B、用聚氯乙烯(PVC)材料作为食品保鲜膜 |
| C、制作膨化食品时可加入过量的膨松剂硫酸铝铵 |
| D、加工香肠时可加入过量的亚硝酸钠使其呈现亮红的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 ,它是由不饱和烃乙的两个分子在一定条件下发生自身加成而得,在此反应中,除获得甲外,同时还获得了另一产物丙,丙是甲的同分异构体,则:乙的结构简式为
,它是由不饱和烃乙的两个分子在一定条件下发生自身加成而得,在此反应中,除获得甲外,同时还获得了另一产物丙,丙是甲的同分异构体,则:乙的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HBr HCl HF |
| B、NH4Cl CH3COONa NH4HCO3 |
| C、NaOH Ca(OH)2 NH3?H2O |
| D、HClO CaF2 Ba(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com