
【题目】利用上述信息,按以下步骤从 ![]() 合成
合成 ![]() .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去) 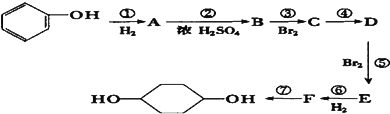
请回答下列问题:
(1)写出 ![]() 的分子式:___
的分子式:___
(2)分别写出B、D的结构简式:B___、D___ .
(3)反应①~⑦中属于消去反应的是___ . (填数字代号)
(4)试写出C→D反应的化学方程式(有机物写结构简式,并注明反应条件):___ .
【答案】 C6H6O ![]()
![]() ②④
②④ ![]() +2NaOH
+2NaOH ![]() +2NaBr+2H2O
+2NaBr+2H2O
【解析】试题分析:本题考查有机推断,有机物结构简式和有机方程式的书写,有机反应类型的判断。![]() 与H2发生加成反应生成A,A的结构简式为
与H2发生加成反应生成A,A的结构简式为![]() ;A在浓H2SO4作用下发生消去反应生成B,B的结构简式为
;A在浓H2SO4作用下发生消去反应生成B,B的结构简式为![]() ;B与Br2发生加成反应生成C,C的结构简式为
;B与Br2发生加成反应生成C,C的结构简式为![]() ;D能与Br2发生反应生成E,E能与H2发生加成反应生成F,则C→D为消去反应,结合
;D能与Br2发生反应生成E,E能与H2发生加成反应生成F,则C→D为消去反应,结合![]() 中两个羟基处于对位,D的结构简式为
中两个羟基处于对位,D的结构简式为![]() ;D与Br2发生1,4-加成反应生成E,E的结构简式为
;D与Br2发生1,4-加成反应生成E,E的结构简式为![]() ;E与H2发生加成反应生成F,F的结构简式为
;E与H2发生加成反应生成F,F的结构简式为![]() ,
,![]() 发生水解反应生成
发生水解反应生成![]() 。
。
(1)![]() 的分子式为C6H6O。
的分子式为C6H6O。
(2)根据上述分析,B的结构简式为![]() ,D的结构简式为
,D的结构简式为![]() 。
。
(3)反应①为苯酚与H2的加成反应,反应②为消去反应,反应③为加成反应,反应④为消去反应,反应⑤为1,4—加成反应,反应⑥为加成反应,反应⑦为取代反应,属于消去反应的是②④。
(4)C→D的化学方程式为![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O。
+2NaBr+2H2O。


科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:(提示:SiO2为难溶于盐酸的固体)

请回答下列问题:
(1)固体a的化学式为________。
(2)在Ⅱ中加过量的烧碱涉及到的反应离子方程式有Fe3+ + 3OH- =Fe(OH)3↓、H+ + OH- =H2O、_________________;Ⅲ中通入足量CO2气体发生反应的离子方程式为________________。
(3)由Ⅲ中得到滤液c的实验操作为_____________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_________________________。
(4)0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合的离子反应方程式为_____________________________________。
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和加入的H2SO4的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类说法正确的是( )
A.纯碱、液态氧、碘酒、稀盐酸依次是盐、单质、混合物、电解质
B.干冰、生石灰、硫酸、碳酸氢铵依次是电解质、氧化物、酸、盐
C.氯化氢、氨气、水银、草木灰依次是电解质、非电解质、单质、混合物
D.冰水、空气、泥水依次是溶液、胶体、浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关![]() 分子结构的下列叙述中正确的是
分子结构的下列叙述中正确的是
①除苯环外的其余碳原子有可能都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上
A. ①② B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于主族元素的说法正确的是( )
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.所有主族元素的最高正价都等于主族序数
D.主族元素的价电子数有可能超过最外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并进行相关探究。
(资料查阅)
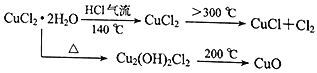
(实验探究)该小组用下图所示装置进行实验(夹持仪器略)。
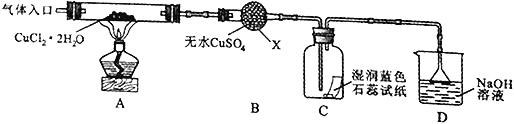
请回答下列问题:
(1)实验操作的先后顺序是a→_______________→e(填操作的编号)。
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(2)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是_______。
(3)装置D中发生的氧化还原反应的离子方程式是________________。
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息
①若杂质是CuCl2,则产生的原因是________________。
②若杂质是CuO,则产生的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19 g·cm-3
HCl的质量分数:36.5%
(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取________mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面(____)
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水(____)
(4)①假设该同学成功配制了0.400 mol·L-1的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是合成抗炎药洛索洛芬钠的关键中间体,它的一种合成路线如下:
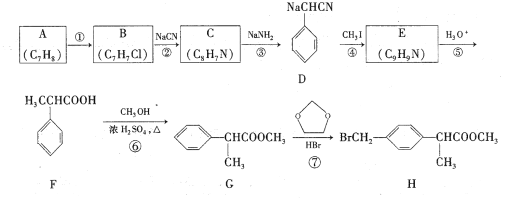
回答下列问题:
(1)A的名称是____,H中官能团名称是____;
(2)反应①的反应条件为____;
(3)反应⑥的化学方程式为________;反应类型为____。
(4)反应⑦除生成H外,还生成了另一种有机产物的结构简式为____。
(5)符合下列条件的G的同分异构体有____种。
I.能发生银镜反应 Ⅱ.苯环上一氯取代物只有一种 Ⅲ.核磁共振氢谱有4组峰
(6)仿照H的合成路线,设计一种由B合成![]() 的合成路线___。
的合成路线___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com