
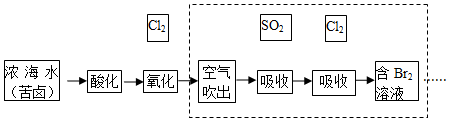
分析 海水蒸发浓缩酸化得到浓缩海水通入氯气氧化溴离子得到含溴单质的混合溶液,利用热空气吹出Br2,被二氧化硫吸收得到含HBr的混合溶液,通入氯气氧化得到溴单质,富集溴元素得到含Br2的混合溶液Ⅱ,蒸馏得到溴单质,
(1)氯气具有氧化性能氧化溴离子生成单质溴;
(2)第1步“吸收”时的反应是二氧化硫和溴单质反应生成硫酸和溴化氢,反应中二氧化硫具有还原性;
(3)①溴单质沸点低易挥发;
②溴单质在四氯化碳中溶解度大;
(4)过程中得到溴单质,通过热空气吹出后用纯碱吸收得到溴酸根和溴离子,在酸溶液中重新得到溴单质是富集溴的过程;
(5)工业可用Na2CO3溶液代替二氧化硫的水溶液吸收Br2,发生反应生成溴化钠、溴酸钠、二氧化碳,结合原子守恒和电子守恒配平书写化学方程式.
解答 解:海水蒸发浓缩酸化得到浓缩海水通入氯气氧化溴离子得到含溴单质的混合溶液,利用热空气吹出Br2,被二氧化硫吸收得到含HBr的混合溶液,通入氯气氧化得到溴单质,富集溴元素得到含Br2的混合溶液Ⅱ,蒸馏得到溴单质,
(1)“氧化”时的离子方程式为:2Br-+Cl2═2Cl-+Br2,
故答案为:2Br-+Cl2═2Cl-+Br2;
(2)第1步“吸收”时的反应是二氧化硫和溴单质反应生成硫酸和溴化氢,反应的离子方程式为:SO2+Br2+2H2O=4H++SO42-+2Br-,反应中二氧化硫具有还原性
故答案为:SO2+Br2+2H2O=4H++SO42-+2Br-;还原;
(3)①直接蒸馏得到溴单质,该操作利用的是溴的沸点低,易挥发,
故答案为:沸点低,易挥发;
②加入四氯化碳萃取,将得到的溴的四氯化碳溶液蒸馏得到溴单质.可以用四氯化碳对溴溶液进行萃取利用,利用的是溴单质在四氯化碳中溶解性大于水中溶解性,
故答案为:溴更易溶于有机溶剂;
(4)过程中得到溴单质,通过热空气吹出后用纯碱吸收得到溴酸根和溴离子,在酸溶液中重新得到溴单质,空气吹出是为了将溴单质从溶液中分离出来,同时增大了溴单质的浓度,用二氧化硫吸收是为了将溴元素进一步富集,用氯气吸收是为了将溴元素转化为最终目标物--溴单质,
故答案为:空气吹出是为了将溴单质从溶液中分离出来,同时增大了溴单质的浓度,用二氧化硫吸收是为了将溴元素进一步富集,用氯气吸收是为了将溴元素转化为最终目标物--溴单质;
(5)工业可用Na2CO3溶液代替二氧化硫的水溶液吸收Br2,发生反应生成溴化钠、溴酸钠、二氧化碳,结合原子守恒和电子守恒配平书写化学方程式为:3 Br2+3 Na2CO3=NaBrO3+3 CO2+5NaBr,反应中若有480g溴物质的量=$\frac{480g}{480g/mol}$=1mol,完全反应,转移电子的物质的量为5mol,
故答案为:3 Br2+3 Na2CO3=NaBrO3+3 CO2+5NaBr;5.
点评 本题考查了海水提溴的生产关系分析判断、过程中反应的原理和作用分析,主要是物质性质和氧化还原反应的理解应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:实验题

 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 酸碱中和反应 | ||
| C. | 灼热的炭与CO2反应 | D. | H2与Cl2的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L的Ca(C1O)2溶液中含C1O数目为2NA | |
| B. | 标准状况下,22.4L戊烷中的氢原子数约为12NA个 | |
| C. | 体积分别为1.0LpH=2的盐酸与硫酸溶液中氢离子数均为0.01NA | |
| D. | 1mol-OH与1molOH-所含电子数均为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都含有 92个中子 | B. | ${\;}_{92}^{235}$U原子核外有143个电子 | ||
| C. | 它们是同种核素 | D. | 它们互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-2,3-二氯戊烷 | B. | 3,3-二甲基-4-乙基戊烷 | ||
| C. | 2,4,6-三氯己烷 | D. | 3-甲基-3-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{10}^{22}$Ne和${\;}_{10}^{20}$Ne是同分异构体 | |
| B. | ${\;}_{10}^{22}$Ne和${\;}_{10}^{20}$Ne属于不同的核素 | |
| C. | ${\;}_{10}^{22}$Ne和${\;}_{10}^{20}$Ne的性质完全相同 | |
| D. | ${\;}_{10}^{22}$Ne转变为${\;}_{10}^{20}$Ne为化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com