
常温下,将1.92 g铜加入到100 mLH2SO4和HNO3的混合液中,Cu全部溶解,放出无色气体,再向溶液中加入足量铁粉,充分反应,此时收集到气体为448 mL(标准状况)的氢气。下列有关结论不正确的是( )
A. 溶解的铁粉为2.8 g
B. 原溶液中(SO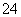 )=0.5 mol·L-1
)=0.5 mol·L-1
C. 原混合溶液中(H+)=1.2 mol·L-1
D. 原溶液中(NO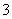 )=0.08 mol
)=0.08 mol
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
SO2、NO是大气污染物。吸收SO2 和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
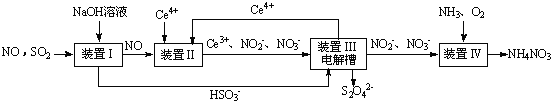
(1)装置Ⅰ中生成HSO3-的离子方程为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如右图所示。
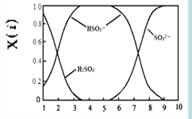
①下列说法正确的是 (填字母序号)。
a.pH=8时,溶液中c(HSO3-) < c(SO32-)
b.pH=7时,溶液中c(Na+) =c(HSO3-)+c(SO32-)
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。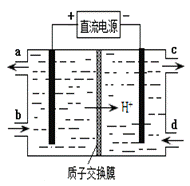
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式 。
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
①生成Ce4+的电极反应式为 。
②生成Ce4+从电解槽的 (填字母序号)口流出。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
铁不能与冷、热水反应,但能与水蒸气反应。资料显示,在不同温度下,还原铁粉与水蒸气反应的产物是不同的,温度低于570 ℃时,生成FeO,高于570 ℃时,生成Fe3O4。老师用如图12-5所示实验装置,完成还原铁粉与水蒸气反应的演示实验。
(1)实验中使用肥皂液的作用是__________________。
(2)甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:
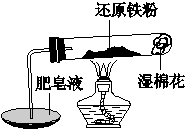
图12-5
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈绿色;有少量气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
根据上述实验,能确定固体中存在的物质是________;不能确定是否存在Fe3O4的原因是___________________。
(3)乙同学设计下列实验方案以确定实验后试管内的固体是否存在Fe3O4:
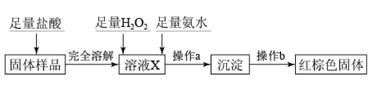
图12-6
①溶液X中发生氧化还原反应的离子方程式为____________________________;足量氨水与金属离子反应的离子方程式为___________________________。
②操作a包括过滤和洗涤,检验沉淀是否已经洗涤干净的操作是___________________________。
③确定是否存在Fe3O4需要测定并记录的实验数据是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的应用正确的是( )
A.液氨汽化时要吸收大量的热,可用作制冷剂
B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟 酸
酸
C.生石灰能与水反应,可用来干燥氯气
D.氯化铝是一种电解质,可用于电解法制铝
查看答案和解析>>
科目:高中化学 来源: 题型:
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是( )
A. 滤液A中的阳离子为Fe3+、Cu2+、H+
B. 样品中Fe元素的质量为2.24 g
C. 样品中CuO的质量为4.0 g
D. =896 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中不仅含有丰富 的非金属元素资源(如氯、溴、碘等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
的非金属元素资源(如氯、溴、碘等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
(1)海水晒盐的原理是:________;写出氯化钠的电子式:________;与Na、Cl同周期,且简单离子半径最小的离子结构示意图:________。
(2)晒出的粗盐常混有MgSO4、CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,②________,③加过量Na2CO3溶液,④________,⑤过滤除去杂质,⑥________,⑦蒸发结晶。
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+、Cr3+等,为富集镁使其转化为MgCl2晶体,必须除去这些杂质离子。
有关资料:
| M(OH) | pH | |
| 开始沉淀 | 沉淀完全 | |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mg(OH)2 | 9.5 | 11.0 |
| Cr(OH)3 | 4.3 | 5.0 |
为了有效除去杂质离子,又不引入新的杂 质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
①先加________,目的是________;
②再加________,目的是________;
③过滤后,为能得到纯净的MgCl2晶体,采用的操作方法是:
_______________ __________________________________
__________________________________
__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.NaCl溶液在电流作用下电离生成Na+与Cl-
B.化合物可分为电解质和非电解质
C.氯化氢溶于水能导电,但液态氯化氢不能导电
D.硫酸钡的水溶液不导电,硫酸钡不是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
工业中硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①②③是工业生产硝酸的主要途径,线路Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。
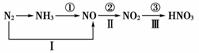
完成下列反应方程式:
写出①的化学方程式:____________________________________________________。
写出Ⅲ的化学方程式:____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com