
| A. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热为-110.5 kJ•mol-1 | |
| B. | 在101kPa下氢气的燃烧热△H=-285.8 kJ•mol-1,则水分解的热化学方程式:2 H2O (l)=2H2 (g)+O2 (g)△H=+285.8 kJ•mol-1 | |
| C. | Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)△H=-2akJ•mol-1,则任何强酸和强碱发生中和反应生成1molH2O(l)的反应热均为-akJ•mol-1 | |
| D. | 1g甲烷完全燃烧生成液态水的过程中放出55.6kJ热量,则CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6kJ•mol-1 |
分析 A.1molC完全燃烧生成二氧化碳时放出的热量为燃烧热;
B.物质的量与热量成正比,互为逆反应时,焓变数值相同、符号相反;
C.稀的强酸与强碱反应生成1mol水的能量为中和热,且生成硫酸钡放热;
D.1g甲烷完全燃烧生成液态水的过程中放出55.6kJ热量,则1mol甲烷完全燃烧生成液态水的过程中放出热量为55.6kJ×16=889.6kJ,以此来解答.
解答 解:A.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,碳的燃烧热为△H<-110.5 kJ•mol-1,故A错误;
B.在101kPa下氢气的燃烧热△H=-285.8 kJ•mol-1,则水分解的热化学方程式为 H2O (l)=H2 (g)+$\frac{1}{2}$O2 (g)△H=+285.8 kJ•mol-1,故B错误;
C.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)△H=-2akJ•mol-1,生成水及硫酸钡均放热,则发生中和反应生成1molH2O(l)的反应热大于-akJ•mol-1,故C错误;
D.1g甲烷完全燃烧生成液态水的过程中放出55.6kJ热量,则1mol甲烷完全燃烧生成液态水的过程中放出热量为55.6kJ×16=889.6kJ,则热化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6kJ•mol-1,故D正确;
故选D.
点评 本题考查热化学方程式的书写,为高频考点,把握物质的量与热量的关系、焓变为解答的关键,侧重分析与应用能力的考查,注意燃烧热、中和热的判断,题目难度不大.


科目:高中化学 来源: 题型:实验题
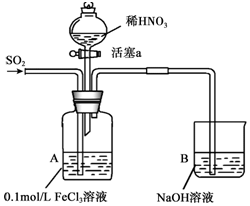 某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验).(忽略氧气对反应的影响)
某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验).(忽略氧气对反应的影响)| 实验序号 | 实验操作 | 实验现象 |
| I | 向A装置中通入一段时间的SO2气体. | A中黄色溶液迅速变成深红棕色,最终变为浅绿色. |
| II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液. | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀. |
| III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色. |
| IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中通入空气. | 溶液变为红色;液面上方有少量红棕色气体生成. |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验步骤 | 预期的现象和结论 |
| ①测定B中实验所用混合溶液的 ②配制具有相同pH的稀硝酸与 BaCl2的混合液并通入适当的N2 ③将SO2通入上述溶液中 | 若出现白色沉淀则假设2成立 若不出现白色沉淀则假设2不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H2SO4溶液中滴入Ba(OH)2溶液至溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| D. | 醋酸溶解鸡蛋壳:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含1molFeCl3溶液水解生成1molFe(OH)3胶体后生成NA个胶体粒子 | |
| B. | 分子数为NA的N2,CO混合气体体积为22.4L,质量为28g | |
| C. | 0.5molFeBr2与足量氯气反应转移的电子数为NA | |
| D. | 足量Zn与一定量的浓硫酸反应,产生22.4L标准状况气体时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌和稀硫酸 | B. | 碳酸钙和硫酸 | ||
| C. | 过氧化氢和二氧化锰 | D. | 硫酸铵和氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学家可以在微观层面上操纵分子和原子,组装分子材料 | |
| B. | 化学是一门具有创造性的科学,化学的特征就是认识分子和制造分子 | |
| C. | 化学是在原子、分子的水平上研究物质的一门自然科学 | |
| D. | 化学注重理论分析、推理,而不需要做化学实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com