
| A、溶液中Na+数目增大,有O2放出 |
| B、溶液中Na+浓度不变,有H2放出 |
| C、溶液中Na+数目减少,有O2放出 |
| D、溶液中Na+浓度增大,有O2放出 |


科目:高中化学 来源: 题型:
 A、B、C、D、E、X为中学常见物质,它们的转化关系如图所示(反应条件未注明).请根据题中信息回答问题.
A、B、C、D、E、X为中学常见物质,它们的转化关系如图所示(反应条件未注明).请根据题中信息回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molCl2与足量Fe反应,转移的电子数为3NA |
| B、0.1mol铁粉与足量的高温水蒸气作用,生成的H2分子数为0.1NA |
| C、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| D、1mol的Na2O2中阴离子个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
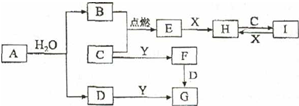 有关物质的转化关系如图所示(部分物质和条件己略去).B、C、E;是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应:G的焰色反应显黄色;I的溶液呈黄色.
有关物质的转化关系如图所示(部分物质和条件己略去).B、C、E;是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应:G的焰色反应显黄色;I的溶液呈黄色.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na2O2+2H2O═4NaOH+O2↑ |
| B、2F2+2H2O═4HF+O2 |
| C、2Na+2H2O═2NaOH+H2↑ |
| D、NaH+H2O═NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分离I2和KMnO4两种固体时,可选择加热使I2升华的方法 |
| B、除去AgI胶体中的NaI时,可将其装在用半透膜做的袋子里,放在流动的蒸馏水中,该分离方法称为渗析 |
| C、粗盐水中含有Ca2+、Mg2+、Fe3+、SO42-等离子,可以通过化学沉淀法除去.如:可以通过加入Ba(NO3)2的方法除去其中的SO42- |
| D、从海带中提取碘单质时,可以将其灼烧后加水溶解过滤,在滤液中加适量氯水将碘元素氧化为I2,最后用乙醇萃取出单质碘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com