
���� ��1��һ�ȴ��飨RCl��������������������Һ��Ϻ���ȣ�������ӦRCl+NaOH��ROH+NaCl�����ữ�����Һ�м�AgNO3��Һʱ��������ӦNaCl+AgNO3=AgCl��+NaNO3���������ĵ�AgNO3����һ�ȴ��飨RCl�������ʵ������ٸ���M=$\frac{m}{n}$����һ�ȴ��飨RCl����Ħ���������ݴ�ȷ�������ȷ��һ�ȴ��飨RCl���ķ���ʽ����д��ͬ���칹�壻
��2��������NaOH����AgNO 3 ��Ӧ�����ɰ�ɫ��AgOH������AgOH���ȶ��������ֽ�Ϊ��ɫAg 2 O���ݴ˽��з�����
��3��±�����е�±�ؾ�����±ԭ�ӵ���ʽ��̼ԭ�ӽ�ϣ�������ˮ��Һ��ֱ�ӵ����X- ��F-��Cl-��Br-��I- �����ʲ�����Ag+ ��Ӧ����������
��� �⣺��1��һ�ȴ��飨RCl��������������������Һ��Ϻ���ȣ�������ӦRCl+NaOH��ROH+NaCl�����ữ�����Һ�м�AgNO3��Һʱ��������ӦNaCl+AgNO3=AgCl��+NaNO3������AgNO3�����ʵ���=0.02L��1mol/L=0.02mol�����ݷ���ʽ��֪n��RCl��=n��AgNO3��=$\frac{2.87g}{143.5g/mol}$=0.02mol����һ�ȴ��飨RCl����Ħ������=$\frac{1.85g}{0.02mol}$=92.5g/mol���������ʽ��Ϊ92.5-35.5=57�������ΪCnH2n+1����14n+1=57�����n=4���ʸ�һ�ȴ���ķ���ʽΪC4H9Cl��
C4H9Cl��ͬ���칹���У�CH3CH2CH2CH2Cl��CH3CH2CHClCH3��CH3CH��CH3��CH2Cl����CH3��3CCl��
�ʴ�Ϊ��CH3CH2CH2CH2Cl��CH3CH2CHClCH3��CH3CH��CH3��CH2Cl����CH3��3CCl��
��2��C4H9Cl��NaOHˮ��Һ���Ⱥ������ữ�ͼ�AgNO3��Һ�����������ɫ��������Ϊ������NaOH����AgNO3 ��Ӧ�����ɰ�ɫ��AgOH������AgOH���ȶ��������ֽ�Ϊ��ɫAg2O���йصĻ�ѧ����ʽΪ��AgNO3+NaOH=AgOH��+NaNO3��2AgOH=Ag 2O+H 2O��
�ʴ�Ϊ����ɫ������AgNO3+NaOH=AgOH��+NaNO3��2AgOH=Ag 2O+H 2O��
��3����������������Һֱ����±������Ӧ������±��������Ϊ±�����е�±�ؾ�����±ԭ�ӵ���ʽ��̼ԭ�ӽ�ϣ�������ˮ��Һ��ֱ�ӵ����X- ��F-��Cl-��Br-��I- �����ʲ�����Ag+ ��Ӧ����������
�ʴ�Ϊ�����ܣ�±�����е�±�ؾ�����±ԭ�ӵ���ʽ��̼ԭ�ӽ�ϣ�������ˮ��Һ��ֱ�ӵ����X- ��F-��Cl-��Br-��I- �����ʲ�����Ag+ ��Ӧ����������
���� �����ѵ㣨1�������л������ʽ��ȷ����ͬ���칹����д�ȣ��ɸ���һ±����������������Һ�������ɵ�����������������Ӧ���ɳ��������ݳ������������ɼ����һ±�����ʽ���������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
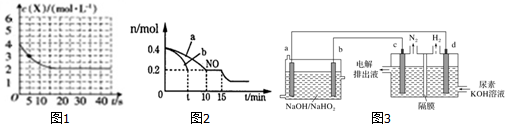
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʳ�Ρ����� | B�� | KSCN��̼������ | C�� | ��ˮ��AgNO3 | D�� | ����ء�����þ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ���� | ������ƽ �������룩 | С�ձ� | ����ǯ | ������ | ҩ�� | ��Ͳ |
| ���� |  |  |  |  |  |  |
| ��� | a | b | c | d | e | f |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
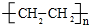 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ��� | ����� |
| 1 | ||
| 2 | ||
| 3 | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
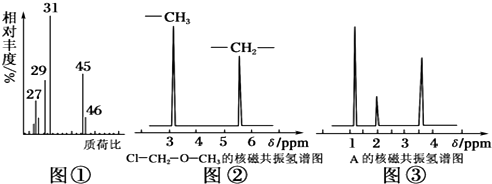
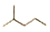 �������ʽΪC6H14��������2-�����飬������2��Ȳͨ���ӳɷ�Ӧ�õ���
�������ʽΪC6H14��������2-�����飬������2��Ȳͨ���ӳɷ�Ӧ�õ���| ʵ�鲽�� | �� �� �� ʵ �� �� �� |
| ��1����ȡA 18.0g������ʹ�������������ܶ�����ͬ������H2��45���� | ��A����Է�������Ϊ90�� |
��2��A�ĺ˴Ź���������ͼ�� | ��A�к���4����ԭ�ӣ� |
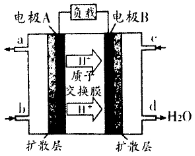
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����2���Ȼ� | B�� | ����1���� | ||
| C�� | ����2���ǻ� | D�� | ͬʱ����1���ǻ���1��ȩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
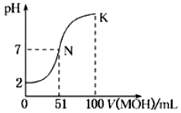
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com