
【题目】请根据要求回答下列问题:
(1)现有某XY3气体a g,它的摩尔质量为b g·mol-1。若阿伏加德罗常数用NA表示,则:该气体的物质的量为________,该气体在标准状况下的体积为__________;该气体溶于水后形成V L溶液,其溶液的物质的量浓度为________________。
(2)等质量的O2和O3所含分子数之比为________,所含原子数之比为_________。
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为__________,R的相对原子质量为__________。
(4)在标准状况下,有CO和CO2组成的混合气体8.96 L,质量是16 g,此混合物中CO和CO2的物质的量比是________,C和O原子个数比是________。
【答案】![]()
![]() L
L ![]() mol/L 3:2 1:1 64g/mol 32 1:3 4:7
mol/L 3:2 1:1 64g/mol 32 1:3 4:7
【解析】
(1)该气体的物质的量为![]() ,该气体在标准状况下的体积为V=nVm;该气体溶于水后形成V L溶液,其溶液的物质的量浓度为
,该气体在标准状况下的体积为V=nVm;该气体溶于水后形成V L溶液,其溶液的物质的量浓度为![]() 。
。
(2)等质量的O2和O3所含分子数之比为N(O2):N(O3)=![]() :
:![]() ,所含原子数之比为
,所含原子数之比为![]() :
:![]() 。
。
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则
n=![]() ,该氧化物的摩尔质量为M=
,该氧化物的摩尔质量为M=![]() ,R的相对原子质量为M-32。
,R的相对原子质量为M-32。
(4)在标准状况下,有CO和CO2组成的混合气体8.96 L,质量是16 g,
![]() ,设CO的物质的量为x,则CO2的物质的量为0.4-x,求出x,即可求出此混合物中CO和CO2的物质的量比,C和O原子个数比。
,设CO的物质的量为x,则CO2的物质的量为0.4-x,求出x,即可求出此混合物中CO和CO2的物质的量比,C和O原子个数比。
(1)该气体的物质的量![]() =
=![]() ,该气体在标准状况下的体积V=nVm=
,该气体在标准状况下的体积V=nVm=![]() L;该气体溶于水后形成V L溶液,其溶液的物质的量浓度
L;该气体溶于水后形成V L溶液,其溶液的物质的量浓度![]() =
=![]() =
=![]() mol/L。答案为:
mol/L。答案为:![]() ;
;![]() L;
L;![]() mol/L;
mol/L;
(2)等质量的O2和O3所含分子数之比为/span>N(O2):N(O3)=![]() :
:![]() =3:2,所含原子数之比为
=3:2,所含原子数之比为![]() :
:![]() =1:1。答案为:3:2;1:1;
=1:1。答案为:3:2;1:1;
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则
n=![]() ,该氧化物的摩尔质量为M=
,该氧化物的摩尔质量为M=![]() =
=![]() =64g/mol ,R的相对原子质量为M-32=64-32=32。答案为:64g/mol;32;
=64g/mol ,R的相对原子质量为M-32=64-32=32。答案为:64g/mol;32;
(4)在标准状况下,有CO和CO2组成的混合气体8.96 L,质量是16 g,
![]() ,设CO的物质的量为x,则CO2的物质的量为0.4-x,
,设CO的物质的量为x,则CO2的物质的量为0.4-x,
28x+44(0.4-x)=16,x=0.1mol,0.4-x=0.3mol,此混合物中CO和CO2的物质的量比为0.1:0.3=1:3,C和O原子个数比为0.4:0.7=4:7。答案为:1:3;4:7。


科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入![]() 一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为
一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为![]() 的
的![]() 溶液,生成的沉淀跟加入的
溶液,生成的沉淀跟加入的![]() 溶液的体积关系如图。(横坐标体积单位是
溶液的体积关系如图。(横坐标体积单位是![]() ,纵坐标质量单位是g)求:
,纵坐标质量单位是g)求:
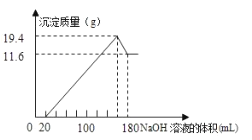
(1)合金中![]() ,
,![]() 的质量_____________
的质量_____________
(2)所用![]() 的物质的量浓度___________
的物质的量浓度___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能。下列说法中不正确的是

A. M极作负极,发生氧化反应
B. 电子流向:M→负载→N→电解质溶液→M
C. N极的电极反应:O2+4H++4e-=2H2O
D. 当N极消耗5.6L(标况下)气体时,最多有NA个H+通过阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体粉末甲由FeSO4、Fe2(SO4)3、CuSO4、CaCO3、SiO2、NaCl中的若干种组成,取一定量的固体甲进行如下实验:
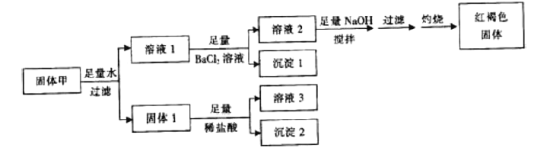
固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g。下列说法正确的是( )
A. 溶液Ⅰ加入KSCN溶液呈红色
B. 取少量溶液2加入酸化的硝酸银溶液,生成白色沉淀,则甲中一定有NaCl
C. 固体Ⅰ与稀盐酸反应时还生成了标准状况下气体1.12L
D. 沉淀2不溶于任何酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气因含有少量H2S等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法不正确的是
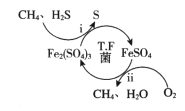
A. 该脱硫过程需要不断添加Fe2(SO4)3溶液
B. 脱硫过程O2间接氧化H2S
C. 亚铁是血红蛋白重要组成成分,FeSO4可用于治疗缺铁性贫血
D. 《华阳国志》记载“取井火煮之,一斛水得五斗盐”,我国古代已利用天然气煮盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①![]()
②![]()
回答下列问题:
(1)A中官能团的名称为________。由F生成H的反应类型为________。
(2)E生成F化学方程式为______________________。
(3)G为甲苯的同分异构体,G的结构简式为________ (写键线式)。
(4)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1,写出2种符合要求的X的结构简式__________。
(5)写出甲苯合成A的合成路线(用流程图表示,无机试剂任选)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O IO![]() →I2 MnO
→I2 MnO![]() →Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
→Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A. H2O2 B. HNO2 C. MnO![]() D. IO
D. IO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种正投入生产的大型蓄电系统,放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是( )
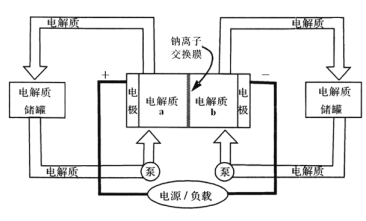
A. 放电时,负极反应为3NaBr-2e-=NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-=Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24 L H2时,b池生成17.40gNa2S4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
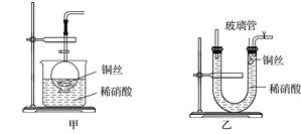
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
(4)以下收集NO气体的装置,合理的是________(填序号)。
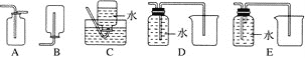
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com