
【题目】下列鉴别方法不可行的是( )
A. 用水鉴别乙醇、甲苯和溴苯
B. 用燃烧法鉴别乙醇、苯和四氯化碳
C. 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D. 用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷
科目:高中化学 来源: 题型:
【题目】下列指定溶液种一定能大量共存的离子组是( )
A. pH=1的溶液中:NH4+、Na+、Fe3+、SO42-
B. 碱性溶液种:Na+、K+、HCO3-、NO3-
C. 中性溶液中:K+、Al3+、Cl-、SO42-
D. Na2S溶液中:SO42-、K+、Al3+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下药品和装置:mg锌片、铁片、稀硫酸、水,设计一个实验,测定锌的相对原子质量(实验是在通常状况下进行的)。请完成下列实验:
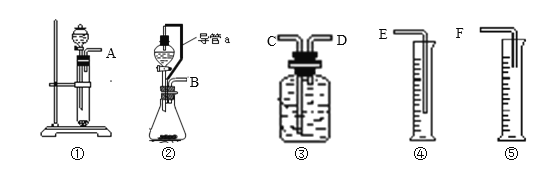
(1)写出该反应的化学方程式 。
(2)所选用装置的连接顺序为(填接口字母) 。
(3)取Wg纯铁片与稀硫酸反应测得生成气体V1mL,该步骤的目的是 。
(4)实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒④,使其中液面与广口瓶中液面相平
C.上下移动量筒⑤,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(5)mg锌片与稀硫酸反应测得生成气体V2mL,则Zn的相对原子质量的数学表达式为 (用上述字母表示)。
(6)假设锌片中含不与酸反应的杂质,实验测得锌的相对原子质量可能比真实值(填“偏大”、“偏小”或“不变”,下同) ;实验结束时,仰视量筒读数,测得值 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况中含微粒数目最多的是
A.0.5molOH—中的电子 B.1mol H2中的H原子
C.0.6mol H2SO4中的O原子 D.1molNa完全反应后失去的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨气的说法正确的是
A. 氨既能用浓硫酸干燥也能用无水CaCl2干燥
B. NH3是电解质,所以氨水能导电
C. NH3可以使干燥的红色石蕊试纸变蓝
D. 用水吸收NH3用如图装置可防止倒吸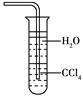
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:

(1)①和③形成的化合物类型为_______ (填“离子”或“共价”)化合物。
(2)元素①的失电子能力比元素⑥_______(填“强”或“弱”),试从原子结构方面解释其原因_______。
(3)⑥单质与氧化铁高温下反应的方程式是______________;工业冶炼⑥的哝璜的化学方程式是________。
⑥的单质与浓NaOH溶液反应的离子方程式是_____________。
(4)实验室现有元素①的单质和⑥的单质,请简要写出比较两者活动性强弱的一种实验方案_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁和高铁酸钾都是常见的水处理剂,下图为制备粗高铁酸钾的工业流程。
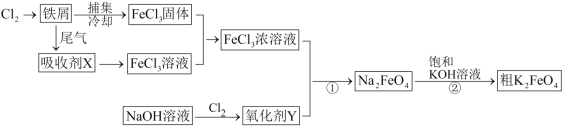
请回答下列问题:
(1)氯化铁做净水剂的原因是(结合化学用语表达) 。
(2)吸收剂X的化学式为 ,氧化剂Y的化学式为 。
(3)碱性条件下反应①的离子方程式为 。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+NaFeO4=K2FeO4+2NaOH,请根据反应原理分析反应能发生的原因 。
(5)K2FeO4在水溶液中易发生反应:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
A.H2O B.稀KOH溶液 C.NH4Cl溶液 D.Fe(NO3)3溶液
除了这种洗涤剂外,一般工业生产还要加入异丙醇作为洗涤剂,你认为选择异丙醇的原因是 。
(6)高铁电池是正在研制中的充电电池,具有电压稳定、放电时间长等优点。以高铁酸钾、二氧化硫和三氧化硫为原料,硫酸钾为电解质,用惰性电极设计成能在高温下使用的电池,写出该电池的正极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一滴香”是有毒物质,被人食用后会损伤肝脏还能致癌。其分子结构如图所示,下列说法正确的是
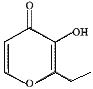
A.该有机物的分子式为C7H7O3
B.该有机物能发生取代、加成和氧化反应
C.1mol该有机物最多能与2mol H2发生加成反应
D.该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com