
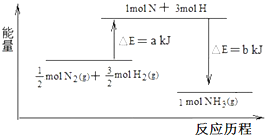 �ڻ�ѧ��Ӧ�У���Ӧ��ת�����������Ȼ���������ı仯��
�ڻ�ѧ��Ӧ�У���Ӧ��ת�����������Ȼ���������ı仯������ ��1��A�����ݻ�ѧ��Ӧ��ʵ���Լ������غ㣻B��ֻ���Է����е�������ԭ��Ӧ������Ƴ�ԭ��أ�C�����ȷ�Ӧ����ʱ��һ��Ҫ���ȣ������ȷ�ӦҲ��һ��Ҫ���ȣ�D�����ݿ��淴Ӧ������������
��2�����ݷ�Ӧ�����������ƽ��д��ѧ����ʽ������n=$\frac{m}{M}$����16gҺ̬N2H4���ʵ���Ϊ0.5mol�����ݶ��ɹ�ϵ�жϣ�0.5molҺ̬N2H4��˫��ˮ��ַ�Ӧ���ɵ�������̬ˮ�ų�320.8kJ����������1molҺ̬����ȫ��Ӧ�ų�641.6KJ��������ע�����ʵľۼ�״̬��ע���ʱ�������ź͵�λ��
��3�����ݷ�Ӧ��=��Ӧ���еļ���֮��-�������еļ���֮�����a��
��� �⣺��1��A����ѧ��Ӧ��ʵ�ʾ��Ǿɻ�ѧ���Ķ��ѣ��»�ѧ�����γɣ��ڻ�ѧ��Ӧ�У���Ӧ��ת��Ϊ�������ͬʱ�����ڷ�Ӧ�����������������ȣ���Ȼ���������ı仯����A��ȷ��
B��ֻ���Է����е�������ԭ��Ӧ������Ƴ�ԭ��أ����Բ����κη��ȷ�Ӧ������Ƴ�ԭ��أ�������кͷ�Ӧ����B����
C�����ȷ�Ӧ����ʱ��һ��Ҫ���ȣ������ȷ�ӦҲ��һ��Ҫ���ȣ���C����
D�����淴Ӧ��һ����������һ�����ȣ�����Ӧ���е�һ���Ⱥ�Ӧ����Ȼת��Ϊ�������D����
��ѡ��A��
��2��16gҺ̬N2H4���ʵ���Ϊn��N2H4��=$\frac{m}{M}$=$\frac{16g}{32g/mol}$=0.5mol��0.5molҺ̬N2H4��˫��ˮ��ַ�Ӧ���ɵ�������̬ˮ�ų�320.8kJ����������1molҺ̬����ȫ��Ӧ�ų�641.6KJ�������������Ȼ�ѧ��Ӧ����ʽΪ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6KJ/mol��
�ʴ�Ϊ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-641.6KJ/mol��
��3���÷�Ӧ���ȣ���Ӧ��=��Ӧ��ļ���-������ļ��ܣ�������������Ӧ���ɰ������Ȼ�ѧ����ʽΪ��$\frac{1}{2}$N2��g��+$\frac{3}{2}$H2��g?NH3��g����H=��a-b��kJ•mol-1����N2��g��+3H2 ��g��=2NH3��g����H=2��a-b��kJ•mol-1=-184kJ•mol-1������a-b=-92������b=1219������a-b=-92��b=1127��
�ʴ�Ϊ��1127��
���� ������Ҫ�����˻�ѧ��Ӧ�������ı仯����Ŀ�ѶȲ���ע��֪ʶ�Ļ��ۣ����շ�Ӧ��=��Ӧ��ļ���-������ļ����ǽ��3���Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��K��Na��Mg��N | B�� | ���ԣ�HNO3��H3PO4��H2SiO3 | ||
| C�� | �ȶ��ԣ�HF��H2O��H2S | D�� | ���ԣ�HClO4��H2SO4��H3PO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ�ͺ���Ȼ��������̼��ȼ�� | |
| B�� | ��չ̫���ܾ��������ڼ�������ЧӦ | |
| C�� | ̫���ܵ�ؿɽ�̫����ת��Ϊ���� | |
| D�� | Ŀǰ�о����˵����ʡ����硱�����ڡ�̫���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��B2��=0.8 mol/��L•s�� | B�� | v��B2��=3mol/��L•min�� | C�� | v��C��=0.6 mol/��L•s�� | D�� | v��A2��=0.4 mol/��L•s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������Ӿ�����ͬ�������Һ�Ԫ��������ͬ�������У��ѧʽ����OH-��H3O+��
������Ӿ�����ͬ�������Һ�Ԫ��������ͬ�������У��ѧʽ����OH-��H3O+�� Fe��OH��3+3H+��H��0��ƽ�������ƶ�����ˮ�����Fe��OH��3�϶�ʱ�;ۼ�Ϊ������
Fe��OH��3+3H+��H��0��ƽ�������ƶ�����ˮ�����Fe��OH��3�϶�ʱ�;ۼ�Ϊ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ȥCO2�е�HCl���� | B�� |  ����NH3 | ||
| C�� |  ���պ����� | D�� |  �Ҵ���ˮ�ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������е��Ļ��ϼ���-3 | |
| B�� | ��Ӧ��ÿ����5.7g AlON��ͬʱ����1.12 L CO | |
| C�� | ��Ӧ�е����������� | |
| D�� | ��Ӧ����������ͻ�ԭ��������ʵ���֮����2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
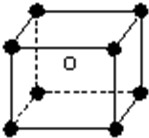 ij���ӻ�����ľ�����ͼ��ʾ����ṹ��������λ�ڴ˾��������ģ�������λ��8�����㣬�����ӻ������У����������Ӹ������ǣ�������
ij���ӻ�����ľ�����ͼ��ʾ����ṹ��������λ�ڴ˾��������ģ�������λ��8�����㣬�����ӻ������У����������Ӹ������ǣ�������| A�� | 1��8 | B�� | 1��4 | C�� | 1��1 | D�� | 1��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com