
| A. | 胶体不均一、不稳定,静置后易产生沉淀;溶液均一、稳定,静置后不产生沉淀 | |
| B. | 布朗运动是胶体粒子特有的运动方式,可以据此将胶体与溶液、悬浊液区分开来 | |
| C. | 光线通过时,胶体发生丁达尔效应,溶液则不能发生丁达尔效应 | |
| D. | 只有胶状物如胶水、果冻类的物质才能称为胶体 |
分析 A.依据胶体的外观特征及介稳性解答;
B.布朗运动是指悬浮在液体或气体中的微粒所作的永不停息的无规则运动;
C.丁达尔效应是胶体特有的性质;
D.胶体有固溶胶和气溶胶液、溶胶之分.
解答 解:A.胶体属于介稳体系,外观特征较均一、较稳定,静置后不产生沉淀,故A错误;
B.胶体,溶液与悬浊液是按照分子的直径的范围来区分的.悬浮微粒不停地做无规则运动的现象叫做布朗运动,与胶体,溶液与悬浊液的区分没有关系,故B错误;
C.丁达尔效应是胶体特有的性质,光线通过时,胶体发生丁达尔效应,溶液则不能发生丁达尔效应,故C正确;
D.胶体有固溶胶和气溶胶液、溶胶之分,如雾属于胶体,故D错误;
故选:C.
点评 本题考查胶体的性质,明确分散系、胶体与溶液的概念及关系是解题的关键,注意丁达尔效应为胶体特有性质,题目难度不大.


 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | Q1>Q2 | |
| B. | 生成物总能量均高于反应物总能量 | |
| C. | 生成1 mol HCl气体时放出Q1 kJ热量 | |
| D. | 1 mol HBr(g)具有的能量小于1 mol HBr(l)具有的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
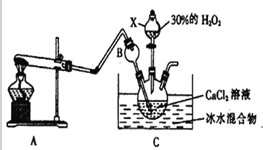
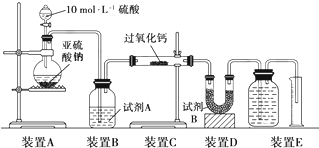
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠的电子式: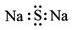 | B. | 中子数为10的氧原子:${\;}_8^{10}O$ | ||
| C. | 硫离子的结构示意图: | D. | HC1O的结构式:H-O-Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥⑦ | B. | ③⑦ | C. | ③⑤⑥ | D. | ③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥⑦ | B. | ③⑤ | C. | ①②④⑦ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:1:2 | C. | 1:2:2 | D. | 4:3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com