
| A. | ②⑤ | B. | ③④ | C. | ②④ | D. | ③⑤ |
分析 ①Cu2+有颜色;
②pH=11的溶液中存在大量的OH-;
③加入铝粉能放出H2的溶液可能呈碱性也可能呈酸性,注意酸性时NO3-的性质;
④由水电离出的c (OH-)=10-13mol•L-1的溶液可能呈酸性或碱性;
⑤能使紫色石蕊试纸变为红色的溶液呈酸性.
解答 解:①Cu2+有颜色,不符合题目无色要求,故错误;
②pH=11的溶液中存在大量的OH-,离子之间不发生反应,可大量共存,故正确;
③加入铝粉能放出H2的溶液可能呈碱性也可能呈酸性,无论呈酸性还是碱性,HCO3-都不能大量共存,故错误;
④由水电离出的c (OH-)=10-13mol•L-1的溶液可能呈酸性或碱性,离子之间不发生任何反应,可大量共存,故正确;
⑤能使紫色石蕊试纸变为红色的溶液呈酸性,酸性条件下S2-、ClO-不能大量共存,故错误.
故选C.
点评 本题考查离子共存,为高频考点,侧重于学生的分析能力的考查,题目难度中等,注意离子的性质,注意分析题中隐含条件,为该类题目常考查方式.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=7的溶液一定是中性 | |
| B. | 若某盐溶液呈酸性或碱性,一定是由于该盐发生了水解反应 | |
| C. | c(H+)<c(OH-)的溶液一定呈碱性 | |
| D. | 在100℃时,纯水的pH<7,因此显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 分子式为H2O和D2O的性质相同 | |
| B. | 相同条件下,等质量的碳按a、b两种途径完全转化,途径a和途径b放出的热能相等 途径a:C$→_{高温}^{H_{2}O}$CO+H2$→_{燃烧}^{O_{2}}$CO2+H2O,途径b:C$→_{燃烧}^{O_{2}}$CO2 | |
| C. | PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | 氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:A13++4NH3•H2O═4NH4++2H2O+A1O2- | |
| B. | 氯化亚铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | NaHCO3溶液和过量的Ba(OH)2溶液混合:2HCO3-+OH-+Ba2+═BaCO3↓+2H2O+CO32- | |
| D. | 用氨水吸收少量二氧化硫:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g | |
| B. | 1 mol Na2O2固体中含离子总数为4NA | |
| C. | 1mol羟基与17 g NH3所含电子数之比为9:10 | |
| D. | 1mol Na2CO3晶体中含 CO${\;}_{3}^{2-}$离子数小于1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22 g 2H218O中含有的质子数为10NA | |
| B. | 电解58.5 g熔融的NaCl,能产生11.2 L氯气(标准状况)、23.0 g金属钠 | |
| C. | 1.00 mol NaCl中,所有Na+的最外层电子总数为10NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C被还原 | B. | C发生氧化反应 | C. | ZnCO3被氧化 | D. | ZnCO3是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
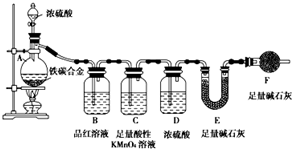 现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com