
 可用尿素
可用尿素 还原(尿素中C元素的化合价为+4价),反应的方程式为:
还原(尿素中C元素的化合价为+4价),反应的方程式为: 。当消耗掉12g尿素时,转移电子的物质的量是 。
。当消耗掉12g尿素时,转移电子的物质的量是 。 ),改流程中发生的主要反应有:
),改流程中发生的主要反应有:
 KJ/mol
KJ/mol 。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
 0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。 转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为 ;已知25℃时,0.05mol/L(NH4)2SO4溶液的
转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为 ;已知25℃时,0.05mol/L(NH4)2SO4溶液的 ,则
,则 = (用含a的代数式表示,已知
= (用含a的代数式表示,已知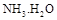 的电离常数
的电离常数 )。
)。 2NO(g)的ΔH,只用到前两个反应,ΔH1-ΔH2即可得到。(4)据图像可知,温度升高平衡逆向移动,所以ΔH<0。T1时,A点对应的α=0.5,据平衡常数表达式可得K=1。因B点与A点温度相同,K不变,可计算出体积为2L。(5)(NH4)2SO4溶液中NH4+水解显酸性,则离子浓度大小顺序为c(NH4+)>c(SO42-)>c(H+)>c(OH-);0.05mol·L-1(NH4)2SO4溶液的pH=a,则c(OH-)=10a-14,依据Kb的表达式和已知数据,可计算出结果为1.7×109-a。
2NO(g)的ΔH,只用到前两个反应,ΔH1-ΔH2即可得到。(4)据图像可知,温度升高平衡逆向移动,所以ΔH<0。T1时,A点对应的α=0.5,据平衡常数表达式可得K=1。因B点与A点温度相同,K不变,可计算出体积为2L。(5)(NH4)2SO4溶液中NH4+水解显酸性,则离子浓度大小顺序为c(NH4+)>c(SO42-)>c(H+)>c(OH-);0.05mol·L-1(NH4)2SO4溶液的pH=a,则c(OH-)=10a-14,依据Kb的表达式和已知数据,可计算出结果为1.7×109-a。

科目:高中化学 来源:不详 题型:单选题
| A.①②⑤ | B.①⑤⑦ | C.①④⑤⑥⑦ | D.③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.右图可表示水分解过程中的能量变化 |
| B.若2C(s)+O2(g)=2CO(g)△H=" -221.0" kJ/mol,则碳的燃烧热为110.5 kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)="2HCl" (g)△H=" -" a kJ/mol, |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该反应的反应热△H=E2-E1 |
| B.a、b分别对应有催化剂和无催化剂的能量变化 |
| C.催化剂能降低反应的活化能 |
| D.催化剂能改变反应的焓变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na和O2 | B.NaOH和CO2 |
| C.Na2O2和CO2 | D.AlCl3和NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有③④ | B.只有①② |
| C.①②③④ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.吸热反应不一定都要加热才反应 |
| B.化学键的断裂和形成是化学反应中能量变化的根源 |
| C.选择燃料只需考虑燃料热值大小 |
| D.若反应物的总键能大于生成物的总键能则反应为吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com