
【题目】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。
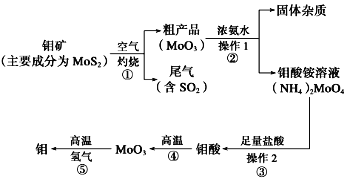
(1)写出在高温下发生反应①的化学方程式______________________________________________
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:________________________________
(3)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有_______________________
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:
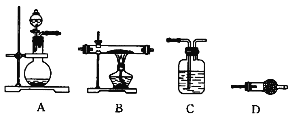
① 请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是___________
② 在烧瓶A中加入少量硫酸铜的目的是____________________________
③ 两次使用D装置,其中所盛的药品依次是____________________、______________________
(5)工业上制备还原性气体CO和H2的反应原理为CO2 + CH4![]() 2CO + 2H2 CH4 + H2O
2CO + 2H2 CH4 + H2O![]() CO + 3H2,含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为________________ (保留两位小数,钼的相对原子质量为96)
CO + 3H2,含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为________________ (保留两位小数,钼的相对原子质量为96)
【答案】2MoS2 + 7O2![]() 2MoO3 + 4SO2 SO2 + 2NH3·H2O=== 2NH4+ + SO32-+ H2O 烧杯、漏斗、玻璃棒 ACBDD 加快反应速率 无水硫酸铜 碱石灰 4.11a g
2MoO3 + 4SO2 SO2 + 2NH3·H2O=== 2NH4+ + SO32-+ H2O 烧杯、漏斗、玻璃棒 ACBDD 加快反应速率 无水硫酸铜 碱石灰 4.11a g
【解析】
根据流程图分析主要反应和主要操作,完成化学方程式、选择所需仪器。根据实验目的,设计相关实验,并防止空气的影响。根据化学反应计量关系,进行有关计算。
(1)据流程图找出反应①的反应物、生成物,并用化合价升降法配平,得2MoS2 + 7O2![]() 2MoO3 + 4SO2;
2MoO3 + 4SO2;
(2)足量的浓氨水吸收SO2生成正盐,离子方程式为SO2 + 2NH3·H2O= 2NH4+ + SO32-+ H2O;
(3)步骤②得固体和溶液,操作1为过滤。步骤③复分解反应能进行,则钼酸难溶于水,操作2为过滤。需要使用的主要玻璃仪器有烧杯、漏斗、玻璃棒;
(4)①制备H2并还原MoO3可证明其还原性,用无水硫酸铜检验氧化产物水,必须对氢气干燥,并防止空气中水汽干扰。故装置连接顺序是ACBDD。
②在烧瓶A中加入少量硫酸铜,可形成原电池,加快生成氢气的速率。
③第一次使用D装置,所盛药品为无水硫酸铜,用于检验氧化产物水。第二次使用D装置,所盛药品为碱石灰等,防止空气中的水汽使无水硫酸铜变蓝。
(5)据CO2 + CH4![]() 2CO + 2H2、CH4 + H2O
2CO + 2H2、CH4 + H2O![]() CO + 3H2,当二氧化碳和水蒸气足量时,CH4 ~ 4(CO + H2);又据MoO3 +3CO=Mo +3CO2、MoO3 +3H2=Mo +3H2O,有3(CO + H2) ~ Mo,故3CH4 ~ 4Mo。则m(Mo)=
CO + 3H2,当二氧化碳和水蒸气足量时,CH4 ~ 4(CO + H2);又据MoO3 +3CO=Mo +3CO2、MoO3 +3H2=Mo +3H2O,有3(CO + H2) ~ Mo,故3CH4 ~ 4Mo。则m(Mo)=![]() ×80%×90%×
×80%×90%×![]() ×96g·mol-1=4.11a g。
×96g·mol-1=4.11a g。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图。根据图示判断,下列结论中不正确的是

A. N点时溶液中的溶质只有NaCl
B. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
C. c(NaOH)=c(HCl)
D. 原混合溶液中c(MgCl2)∶c(AlCl3)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
(1)①已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=196.6 kJ·mol–1
2SO3(g) ΔH=196.6 kJ·mol–1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=113.0 kJ·mol–1
2NO2(g) ΔH=113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3(g)和NO的热化学方程式 。
②一定条件下,将NO2与SO2以体积比1:2置于2L密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO2的同时生成1 molNO2
(2)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO ( g ) + 2H2 ( g ) ![]() CH3OH ( g ) △H=-116kJ/mol
CH3OH ( g ) △H=-116kJ/mol
一定条件下在2L密闭容器中,将1 mol CO与3 mol H2的混合气体在催化剂作用下发生反应生成甲醇。
① 2min时测得生成CH3OH 0.2mol,则0~2min的平均反应速率v(H2)= 。
②反应5min后达到平衡,若平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加
d.重新平衡c(H2)/c(CH3OH)减小
(3)在密闭容器中充有1mol CO与2 mol H2,在催化剂作用下反应生成甲醇,CO的转化率(α)与温度(T)、压强(P) 的关系如图所示。
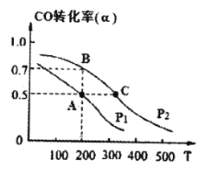
A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“>”、“<”或“=”)。
② 若A点时容器的体积为1 L,则该温度下B的平衡常数 KB= ,C点的平衡常数KC KB(填“<”、“>”或“=”)。
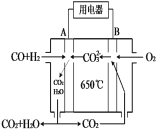
(4)下图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3共熔混合物为电解质。A为电池的 极(选填“正”或“负”),写出B极电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子核外p电子数比s电子数少1,C为金属元素且原子核外p电子数和s电子数相等,D元素的原子核外所有p轨道全充满或半充满。
(1)写出A、B元素的元素符号:A________,B________。
(2)写出C元素基态原子核外电子排布式:C______________________________。
(3)写出D元素基态原子核外电子轨道表示式:D_____________________________。
(4)写出B、C两种元素单质在一定条件下反应的化学方程式:___________________。
(5)写出B元素单质和氢化物的电子式:单质________,氢化物__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种元素的基态原子的电子排布式如下:
![]()
则下列有关比较中正确的是( )
A. 第一电离能:④>③>②>① B. 原子半径:④>③>②>①
C. 电负性:④>③>②>① D. 最高正化合价:④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次减小,其中只有Z为金属元素,X、Y、Z同周期且位于不同奇数族,Z、W同主族,Y、Z的原子序数相差4。下列说法正确的是( )
A. W的简单阴离子半径一定大于Z的简单阳离子半径
B. 非金属性:X>Y,所以X和Y分别对应含氧酸的酸性:X一定强于Y
C. X、 Y形成的单质一定都是双原子分子
D. Z、W形成化合物的电子式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是
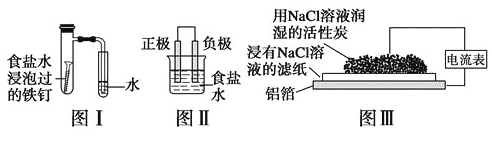
A. 按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B. 图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C. 铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D. 图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色
B. 有机物![]() 的消去产物只有2种
的消去产物只有2种
C. 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH-COOCH3
D. 可用溴水鉴别已烯、四氯化碳和乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。

回答下列问题:
(1)反应的△H_______0(填“大于”或“小于”) ;100℃时,体系中各物质浓度随时间变化如上图所示。在0-60s时段,反应速率v(N2O4)为______mol·L-1·s-1;反应的平衡常数K1为________。
(2) 100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。
a: T______100℃ (填“大于”或“小于”) ,判断理是_______
b:计算温度T时反应的平衡常数K2(要求写出计算过程)__________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向______(填“正反应”或“逆反应”)方向移动,判断理由是__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com