
【题目】利用反应 NO2+NH3→N2+H2O(未配平)制作下面装置图所示的电池,用以消除氮氧化物的污染。下列有关该电池说法一定正确的是 ( )
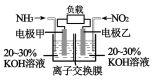
A.电极乙为电池负极
B.离子交换膜为质子交换膜
C.负极反应式为 2NH3-6e-+6OH-=N2↑+6H2O
D.28.0L(标准状况)NO2 完全被处理,转移 4mol 电子
【答案】C
【解析】
根据题干信息,反应NO2+NH3→N2+H2O中,NO2中N元素化合价降低,得到电子,发生还原反应,NH3中N元素化合价升高,失去电子,发生氧化反应,则电极甲为负极,电极乙为正极,据此分析解答。
A.由上述分析可知,电极乙为原电池的正极,A选项错误;
B.该电池中,NO2在正极得到电子,发生还原反应,电极反应式为2NO2+4H2O+8e-===N2+8OH-,OH-向负极移动,则离子交换膜为阴离子交换膜,B选项错误;
C.NH3在负极失去电子,发生氧化反应,电极反应式为2NH3-6e-+6OH-=N2↑+6H2O,C选项正确;
D.由负极反应2NO2+4H2O+8e-===N2+8OH-,转移4mol电子需处理1molNO2,标准状况下NO2为液体,28.0L的物质的量未知,D选项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】(1)铁元素是构成人体的必不可少的元素之一,缺铁会影响到人体的健康和发育,最大的影响是缺铁性贫血。此类病人需要服用补铁药品。

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________。
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_______性。下列不能实现上述转化的物质是_______。
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了________性和________性,则生成1分子NO转移电子数为________;56g Fe参加反应时,被还原的HNO3为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】450℃时,在某恒容密闭容器中存在反应:C(s)+2NO(g)![]() N2(g)+CO2(g),下列说法能作 为判断该反应达到化学平衡状态标志的是
N2(g)+CO2(g),下列说法能作 为判断该反应达到化学平衡状态标志的是
A. 容器内压强保持不变B. v正(N2)=2v逆(NO)
C. N2与CO2的物质的量之比为1∶1D. 容器内混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍及其化合物是重要的合金材料和催化剂。
(1)基态镍原子的价电子排布式为___,它核外有___种运动状态不同的电子。
(2)Ni2+可以形成多种配离子,比如[Ni(NH3)4]2+、[Ni(CN)4]2-等。CN-中碳原子的杂化方式为___,与CN-互为等电子体的一种分子是___。[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角___(填“大”、“小”或“相等”),原因是___。
(3)元素铜与镍的第二电离能分别为:I2(Cu)=1958kJ/mol、I2(Ni)=1753kJ/mol,铜的第二电离能更大的原因是___。
(4)NiO的晶体结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为___。
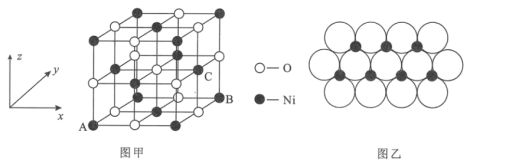
(5)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为apm,设阿伏加德罗常数的值为NA,每平方米面积上分散的该晶体的质量为___g(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生命科学常用图示表示微观物质的结构,图中甲、乙、丙分别表示植物细胞中常见的三种有机物,则甲、乙、丙可分别表示( )

A.DNA、蛋白质、糖原B.蛋白质、核酸、蔗糖
C.多肽、RNA、淀粉D.DNA、RNA、纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在工农业生产及航天航空业中具有广泛的用途。回答下列问题:
⑴NF3为无色、无味的气体,可用于微电子工业,该物质在潮湿的环境中易变质生成HF、NO、HNO3。该反应中氧化剂与还原剂的物质的量之比为______,NF3在空气中泄漏时很容易被观察到,原因是_______。
⑵汽车尾气中催化剂可将NO、CO转化成无害气体。
化学键 | C≡O | NO中氮氧键 | N≡N | CO2中C=O键 |
键能/kJ·mol1 | 1076 | 630 | 945 | 803 |
2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH
①ΔH=______________________________kJ·mol1。
②该反应的平衡常数与外界因素X(代表温度、压强、![]() 或催化剂接触面)关系如下图所示。
或催化剂接触面)关系如下图所示。
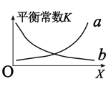
X是______,能正确表达平衡常数K随X变化的曲线是_______(填:a或b)。
⑶在一定温度和催化剂作用下,8NH3(g)+8NO(g)+2NO2(g)9N2(g)+12H2O(g)在2L密闭容器中通入4molNH3、4molNO、nmolNO2,经10分钟时达到平衡时,c(NH3)=0.5mol·L1,c(NO2)=0.25mol·L1。
①n=_____;
②υ(NO)=______;
③NH3的平衡转化率为_________。
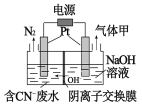
⑷用电解法将某工业废水中CN-转变为N2,装置如下图所示。电解过程中,阴极区电解质溶液的pH将____________(填:增大、减小或不变)。阳极的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的氢气在氯气中燃烧,所得混合物用100ml 3.0mol/L的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
(1)写出实验室制氯气的化学方程式_______________________________,氧化剂与还原剂的物质的量之比为 ________。
(2)氯气与氢氧化钠溶液反应的离子方程式为 _______________________________ 。
(3)所得溶液中Cl-的物质的量为_____________mol。
(4)原混合物中氯气和氢气的物质的量之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)相对分子质量为72且沸点最低的烷烃的结构简式为________。
(2)键线式![]() 表示的分子式为_________;1 mol该烃完全燃烧需消耗氧气的物质的量为_____mol。
表示的分子式为_________;1 mol该烃完全燃烧需消耗氧气的物质的量为_____mol。
(3)松油醇![]() 含有的官能团的名称为__________________.
含有的官能团的名称为__________________.
(4)分子式为C4H4且含两种官能团的链状有机物的结构简式为____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2催化加氢制甲醇,是极具前景的温室气体资源化研究领域。在某CO催化加氢制甲醇的反应体系中,发生的主要反应有:
i.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
ⅱ.CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2=+41.2kJ·mol-1
CO(g)+H2O(g) △H2=+41.2kJ·mol-1
ⅲ.CO(g)+2H2(g) ![]() CH3OH(g) △H3
CH3OH(g) △H3
(1)△H3________ kJ·mol-1
(2)5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
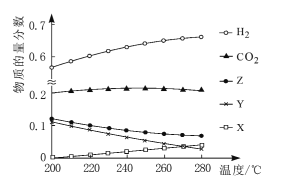
①体系中CO2的物质的量分数受温度的影响不大,原因是____。
②250℃时,反应ii的平衡常数____1(填“>”“<”或“=”)。
③下列措施中,无法提高甲醇产率的是____(填标号)。
A 加入适量CO B 增大压强 C 循环利用原料气 D 升高温度
④如图中X、Y分别代表____(填化学式)。
(3)反应i可能的反应历程如下图所示。

注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV)。其中,TS表示过渡态、*表示吸附在催化剂上的微粒。
①反应历程中,生成甲醇的决速步骤的反应方程式为____。
②相对总能量E=____(计算结果保留2位小数)。(已知:leV=1.6×10-22kJ)
(4)用电解法也可实现CO2加氢制甲醇(稀硫酸作电解质溶液)。电解时,往电解池的____极通入氢气,阴极上的电极反应为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com