
【题目】利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)制备铁红,大致生产过程如下 
请回答:
(1)验滤液A 中含有Fe2+的方法是 .
(2)滤液A→B发生反应的离子方程式为 .
(3)在空气中煅烧FeCO3的方程式为 .
【答案】
(1)取少量滤液A于试管中,向试管中滴加酸性高锰酸钾溶液,若溶液褪色,则说明存在Fe2+
(2)2Fe3++Fe=3Fe2+
(3)4FeCO3+O2 ![]() 2Fe2O3+4CO2
2Fe2O3+4CO2
【解析】解:(1)Fe2+具有还原性,可与高锰酸钾发生氧化还原反应而使高锰酸钾溶液褪色,检验方法为取少量滤液A于试管中,向试管中滴加酸性高锰酸钾溶液,若溶液褪色,则说明存在Fe2+ , 所以答案是:取少量滤液A于试管中,向试管中滴加酸性高锰酸钾溶液,若溶液褪色,则说明存在Fe2+;(2)滤液A→B为铁离子与铁的反应,发生反应的离子方程式为2Fe3++Fe=3Fe2+ , 所以答案是:2Fe3++Fe=3Fe2+;(3)在空气中煅烧FeCO3生成氧化铁和二氧化碳,亚铁被氧化,应有氧气参加反应,方程式为4FeCO3+O2 ![]() 2Fe2O3+4CO2 ,
2Fe2O3+4CO2 ,
所以答案是:4FeCO3+O2 ![]() 2Fe2O3+4CO2 .
2Fe2O3+4CO2 .


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 离子键就是阴阳离子间的静电引力
B. 所有金属元素与所有非金属元素间都能形成离子键
C. 钠原子与氯原子结合成氯化钠后体系能量降低
D. 在离子化合物CaCl2中,两个氯离子间也存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施不符合节能减排的是( )
A.大力发展火力发电,解决广东电力紧张问题
B.在屋顶安装太阳能热水器为居民提供生活用热水
C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)如图所示,在一个小烧杯里加入研细的20g Ba(OH)28H2O晶体.将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入10g NH4Cl晶体,并用玻璃棒快速搅拌. 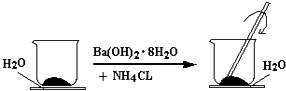
①实验中玻璃棒作用是;
②写出有关反应的化学方程式:;
从四大基本反应类型分析,该反应类型是;
③实验现象可以说明该反应的反应物的总能量(填“大于”或“小于”)生成物的总能量
(2)氢气是未来最理想的能源之一,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O ![]() 2H2↑+O2↑.制得的氢气可用于燃料电池. 试回答下列问题:
2H2↑+O2↑.制得的氢气可用于燃料电池. 试回答下列问题:
①海水分解生成的氢气用于燃料电池时,实现能转变为能.水分解时,断裂的化学键为键,分解海水的反应属于反应(填“放热”或“吸热”).
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2﹣﹣4e﹣═2H2O;B极:O2+4e﹣═2O2﹣ , 则A极是电池的极;电子从该极(填“流入”或“流出”).
③有人以化学反应:2Zn+O2+4H+═2Zn2++2H2O为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作.则原电池的负极上发生反应的电极反应式为 .
(3)若氢气的燃烧过程中,破坏1molH2中的化学键消耗的能量为Q1kJ,破坏1molO2中的化学键为Q2kJ,形成1molH2O中的化学键释放的能量为Q3 . 下列关系式正确的是
A.Q1+Q2>Q3
B.Q1+Q2<Q3
C.2Q1+Q2>2Q3
D.2Q1+Q2<2Q3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不可能是原电池反应的是( )
A.Fe+2H+=Fe2++H2↑
B.H++OH﹣=H2O
C.2H2+O2=2H2O
D.Fe2++Zn=Fe+Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人造地球卫星用到的一种高能电池﹣﹣银锌蓄电池,其电池的电极反应式为:Zn+2OH﹣﹣2e﹣═ZnO+H2↑,Ag2O+H2O+2e﹣═2Ag+2OH﹣ . 据此判断氧化银是( )
A.负极,被氧化
B.正极,被还原
C.负极,被还原
D.正极,被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com