
【题目】如下图所示,△H1=-393.5 kJ· mol-1,△H2=-395.4kJ· mol-1,下列说法或表示式正确的是

A. C(s、石墨)== C(s、金刚石) △H= +1.9 kJ· mol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 石墨的总键能比金刚石的总键能小1.9 kJ
【答案】A
【解析】先根据图写出对应的热化学方程式,接着根据盖斯定律写出石墨转变成金刚石的热化学方程式,最后根据物质的能量越低越稳定来解答。
A、由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJmol-1
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJmol-1
利用盖斯定律将①-②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJmol-1,A正确;
B、石墨和金刚石是不同的两种物质,石墨和金刚石的转化是化学变化,B错误;
C、由C(S,石墨)=C(S,金刚石)△H=+1.9kJmol-1,金刚石能量大于石墨的总能量,物质的量能量越高越不稳定,则石墨比金刚石稳定,C错误;
D、由C(S,石墨)=C(S,金刚石)△H=+1.9kJmol-1,1mol石墨的总键能比1mol金刚石的总键能大1.9 kJ,D错误;答案选A。


科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述不正确的是
A. 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体
B. 煤的干馏和石油的分馏均属化学变化
C. ![]() 可用于文物年代的鉴定,
可用于文物年代的鉴定,![]() 与
与![]() 互为同位素
互为同位素
D. 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国许可使用的食盐抗结剂目前有:亚铁氰化钾、磷酸钙、二氧化硅和微晶纤维素。卫生部规定食盐中亚铁氰化[K4Fe(CN)6]的最大使用量为10mgkgˉ1.
(1)基态钾原子核外能量最高的电子所在能级的轨道数目为__________,K4Fe(CN)6中Fe2+的外围电子排布图为_________________。
(2)K4Fe(CN)6中存在_____________(填序号)。
A.离子键 B.非极性键 C.配位键 D.σ键 E.π键
(3)写出和CN-互为等电子体的离子的电子式为______________________
(4)磷酸钙中磷酸根的空间构型为______________,二氧化硅晶体中硅原子的杂化方式为_____
(5)亚铁氰化钾溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与CN-是等电子体的气态化合物,反应化学方程式为_______________。
(6)FeO晶体的晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为428pm,则该晶体的密度为____g/cm3 (列出计算式即可,用NA 表示阿伏伽德罗常数的值)。
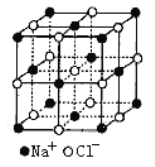
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是( )
A. 纯碱溶液去油污
B. 将三氯化铁溶于盐酸中配制三氯化铁溶液
C. 加热氯化铁溶液颜色变深
D. 硫酸氢钠溶液显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂动力电池(LiFePO4电池)是一种新型动力电池。电池的内部结构如图所示。中间是聚合物的隔膜,它把正极与负极隔开,Li+可以通过而e-不能通过。该电池的总反应式为:Li1-xFePO4+LixC6![]() C6 +LiFePO4 (注:LixC6是单质Li附在碳电极上的一种形式)。下列关于该电池的叙述错误的是
C6 +LiFePO4 (注:LixC6是单质Li附在碳电极上的一种形式)。下列关于该电池的叙述错误的是
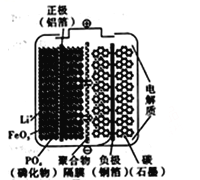
A. 放电时, LixC6在负极上失电子发生氧化反应
B. 在充电时,正极中的Li+通过聚合物隔膜向负极迁移
C. 放电时,正极反应式为Li1-xFePO4+xLi+= LiFePO4-xe-
D. 若用该电池电解精炼铜,阴极质量增重19.2kg时,则电池中通过聚合物隔膜的Li+数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾是一种高效的多功能水处理剂,具有强氧化性。制备高铁酸钾方法很多。
(1)干法制备高铁酸钾。将Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物。此制备反应中,氧化剂与还原剂的物质的量之比为_____________________。
(2)湿法制备高铁酸钾。工业上常采用NaClO氧化法生产,原理如下:
a.3NaClO+2Fe(NO3)3+ 10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
b.Na2FeO4+2KOH =K2FeO4+2NaOH
主要的生产流程如图:
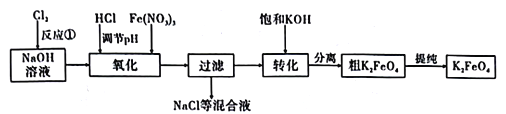
①流程图中“转化”是在某低温下进行的,说明此温度下的溶解度S(K2FeO4)_____S(Na2FeO4)(填“>”“<”或“=”)。
②湿法制备中,反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。如图,图甲为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图乙为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。工业生产中最佳温度为_________℃,此时Fe(NO3)3与NaClO 两种溶液最佳质量浓度之比为______________。

③若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:_____________________。若Fe( NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式为__________________________________。
(3)K2FeO4在水溶液中易水解:4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2↑。
4Fe(OH)3+8OH-+3O2↑。
①在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用__________溶液(填序号)。
A.H2O B.CH3COOK、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
②K2FeO4在处理水的过程中所起的作用有_______________________。
(4)室温下,向含有Fe3+的CuSO4溶液中加入Cu(OH)2可使Fe3+转化为Fe(O H)3沉淀,从而除去Fe3+。该反应的平衡常数为_____________________。(已知常温下的溶度积常数:Ksp[Cu(OH)2]=2.0×10-20, Ksp[Fe(OH)3]=4.0×10-38)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成中的一种重要还原剂—铝氢化钠(NaAlH4),其合成线路如图所示:

(1)已知:AlCl3的熔点为190℃,沸点为178℃,在潮湿空气中会水解。某实验小组利用图所示装置制取无水AlCl3。
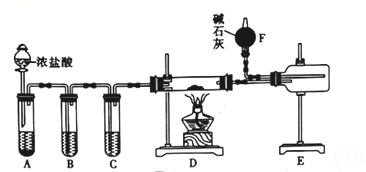
①A中所盛装的固体试剂的化学式为________________________。
②装置F的作用是_________________________________________________。
(2)若改变A、B、D 中的试剂就可以用该装置制取NaH,如制取中操作不当,制得的NaH中可能含有的主要杂质为__________(填序号)。
a.Na b.NaOH c.Na2O2 d.Na2CO3
(3)AlCl3与NaH 反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因是____________________________________。
(4)铝氢化钠遇水发生剧烈反应,甚至爆炸,其反应的化学方程式为__________________________。
(5)现设计如图所示四种装置,测定铝氢化钠粗产品的纯度(只含NaH杂质)。
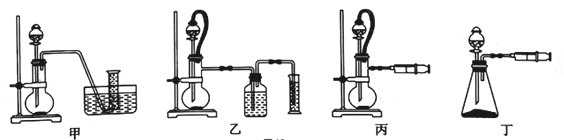
从简约性、安全性和准确性考虑,最适宜的装置是_________(填编号)。铝氢化钠与水完全反应,读气体体积时需冷却至室温,则冷却至室温的标志是__________________________________。
若称取24.0g样品与水完全反应后,测得生成气体在标准状况下的体积为38.08L,则样品中铝氢化钠的质量分数为_______________。(结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化学反应中的焓变(Δ H)与反应物和生成物的键能(E)有关。下表给出了一些化学键的键能:
化学键 | H-H | N≡N | O=O | O-H | N-H |
键能(kJ/mol) | 436 | 942 | 500 | 463 | a |
已知工业合成氨: N2(g)+3H2(g)![]() 2NH3(g) Δ H= -92.4 kJ· mol-1, 请回答下列问题:
2NH3(g) Δ H= -92.4 kJ· mol-1, 请回答下列问题:
(1)表中 a = ______ kJ· mol-1
(2)1 mol N2和 3 mol H2充分反应,放出的热量______92.4 kJ(填“>”、“<”或“=”)。
II.随着人类对温室效应和资源短缺等问题的重视,如何降低大气中 CO2的含量及有效地开发利用CO2,引起了普遍的重视。
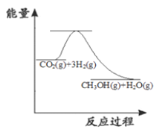
(1)目前工业上有一种方法是用 CO2来生产甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。下图表示该反应进行过程中能量的变化,该反应是_____(填“吸热”或“放热”)反应;
CH3OH(g)+H2O(g)。下图表示该反应进行过程中能量的变化,该反应是_____(填“吸热”或“放热”)反应;
(2)下列各项中,能说明 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)已达到平衡的是____(填选项)。
CH3OH(g)+H2O(g)已达到平衡的是____(填选项)。
A.恒温、恒容条件下,容器内的压强不发生变化
B.一定条件下,CH3OH 分解的速率和 CH3OH 生成的速率相等
C.一定条件下,单位时间内消耗 1 mol CO2,同时生成 1 mol CH3OH
D.一定条件下,H2O(g)的浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组微粒或物质:
A、O2和O3
B、 ![]() 和
和 ![]()
C、CH3CH2CH2CH3和 ![]()
D、 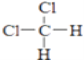 和
和 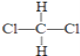
E、CH3CH2CH2CH3和 ![]()
(1)________组两种微粒互为同位素;
(2)________组两种物质互为同素异形体;
(3)________组两种物质属于烃;
(4)________组两物质互为同分异构体;
(5)________组两物质是同一物质.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com