
28.下图对三种不同类型汽车(以序号1、2、3表示)的废气排放情况进行了比较,这三种汽车分别是以汽油为燃料的汽车、以天然气(主要成份是甲烷)为燃料的汽车和电动汽车。请判断其中序号为1的是
汽车,序号为3的是 汽车。
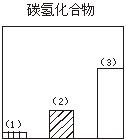
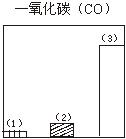
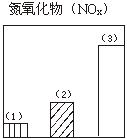
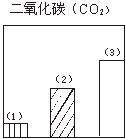
29.图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3白色沉淀的质量与二氧化碳体积之间的关系曲线。试回答:
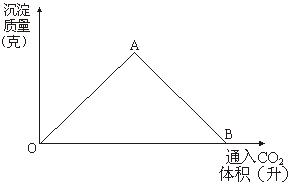
OA段曲线和AB段曲线所表示的反应方程式是
OA:
AB:
A点时已参加反应的CO2和Ca(OH)2的物质的量之比为 。
B处溶液中存在的浓度较大的两种离子是 和 。(填离子符号)
将B处生成的溶液煮沸,可见到的现象是 。
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:高中化学 来源:必修二训练化学苏教版 苏教版 题型:022
下面是关于汽车燃料及其燃烧产物性质的问题:
下图对三种不同类型汽车(以序号①②③表示)的废气排放情况进行比较.这三种汽车分别是以汽油为燃料的汽车,以天然气为燃料的汽车和电动汽车.请判断序号①是________汽车,③是________汽车.

查看答案和解析>>
科目:高中化学 来源:必修二高手化学苏教版 苏教版 题型:022
下面是关于汽车燃料及其燃烧产物性质的问题:
(1)下图对三种不同类型汽车(以序号(1)(2)(3)表示)的废气排放情况进行比较.这三种汽车分别是以汽油为燃料的汽车,以天然气为燃料的汽车和电动汽车.
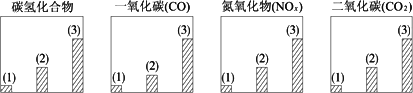
请判断序号(1)是________汽车,(3)是________汽车.
(2)如图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3沉淀的质量与二氧化碳体积之间的关系曲线.试完成下列问题:
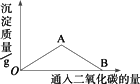
OA段曲线和AB段曲线表示的反应方程式是:
OA:__________________________________;
AB:__________________________________.
A点参加反应的CO2和Ca(OH)2的物质的量之比为________.B处溶液中存在的浓度较大的两种离子是________和________(填离子符号).将B处生成的溶液煮沸,可见到的现象是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下图对三种不同类型汽车(以序号①②③表示)的废气排放情况进行比较。这三种汽车分别是以汽油为燃料的汽车,以天然气为燃料的汽车和电动汽车。请判断序号①是___________汽车,③是______________汽车。

(2)下图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3沉淀的质量与二氧化碳体积之间的关系曲线。试完成下列问题:

OA段曲线和AB段曲线表示的反应方程式是:
OA:______________________________________________________________;
AB:______________________________________________________________;
A点时参加反应的CO2和Ca(OH)2的物质的量之比为______________________________;
B处溶液中存在的浓度较大的两种离子是_______________和___________。(填离子符号)
将B处生成的溶液煮沸,可见到什么现象?______________________________________。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题

 2HI(g),实验测得起始及平衡时的有关数据如表所示:
2HI(g),实验测得起始及平衡时的有关数据如表所示: 
 2HI(g) △H=-23.15kJ/mol
2HI(g) △H=-23.15kJ/mol 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com