
【题目】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。
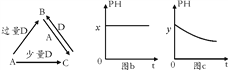
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_______。
(2)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间 t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D的化学式为 _________________________________________;
②若图c符合事实,则其pH变化的原因是 _____________________________________(用离子方程式表示)
【答案】 3Fe2++4H++NO3-═3Fe3++NO↑+2H2O CO2 2HSO3-+O2=2H++2SO4 2-
【解析】本题考查物质的推断,D是某强酸的稀溶液,A为金属单质,A与少量的D反应,与足量D反应产物是不同,根据转化关系,A为Fe,D为HNO3,C为Fe(NO3)2,因此C和D反应的离子方程式为3Fe2++4H++NO3-═3Fe3++NO↑+2H2O;(2)①A为强碱,D为气态氧化物,即为酸性氧化物,D为SO2或CO2,图bpH不变,因此D为CO2,因为+4价S具有还原性,溶液被空气中的氧气氧化;②D为SO2,B为NaHSO3,NaHSO3容易被空气氧化成,因此离子反应方程式为2HSO3-+O2=2H++2SO42-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作都要用玻璃棒:①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体,其中玻璃棒作用相同的是( )
A. ①和② B. ①和③ C. ①和④ D. ③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,1 molX和n mol Y在容积为2L的密闭容器中发生如下反应:X(g)+Y(g)![]() 2Z(g)+M(s),5min后达到平衡,此时生成0.2 mol Z。下列说法正确的是
2Z(g)+M(s),5min后达到平衡,此时生成0.2 mol Z。下列说法正确的是
A.若将容器压缩时,正逆反应速率均不变
B.5 min内平均反应速率v(X)=0.02 mol/(L·min)
C.向平衡后的体系中加入l molM(s),平衡向逆反应方向移动
D.当混合气体的质量不再发生变化时,说明反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期主族元素,且原子序数依次增大。已知W元素的原子形成的离子是一个质子;X、Y在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;Z为同周期中原子半径最大的元素。下列有关说法正确的是
A. 四种元素均为非金属元素
B. W与X、Y形成的最简单分子的沸点:X>Y
C. Y、Z形成的化合物中只含离子键
D. W、Y、Z形成的化合物的电子式为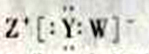
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应H2(g)+Cl2(g)═2HCl(g) 的发生过程能量变化如下所示:
![]()
下列说法错误的是
A.H﹣H键比Cl﹣Cl键稳定
B.△H=﹣184.5 kJmol﹣1
C.正反应活化能比逆反应活化能高
D.在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时△H相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com