
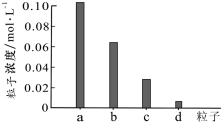
 �����£���0.20mol/L H2X��Һ��0.20mol/L NaOH��Һ�������ϣ�������ҺpH=3.6�������μ�NaOH��Һ��pH=4.0ʱ����������Ũ������ͼ��ʾ������˵��������ǣ�������
�����£���0.20mol/L H2X��Һ��0.20mol/L NaOH��Һ�������ϣ�������ҺpH=3.6�������μ�NaOH��Һ��pH=4.0ʱ����������Ũ������ͼ��ʾ������˵��������ǣ�������| A�� | ͼ��a����Na+��d����H2X���� | |
| B�� | H2XΪ��Ԫ���ᣬHX-�ĵ���̶ȴ���ˮ��̶� | |
| C�� | �����ҺpH=3.6ʱ��c��H+��+c��H2X��=c��X2-��+c��OH-�� | |
| D�� | �����μ�NaOH��Һ��pH=7.0ʱ��c��Na+����c��HX-��+2c��X2-�� |
���� ��H2X��NaOH��Һ���������Ũ��0.2mol/L��ϣ�H2X+NaOH=NaHX+H2O��������Һ��Na+Ũ�ȵ�����0.1mol/L������ҺpH=3.6��˵��NaHX�ǵ���̶ȴ���ˮ��̶ȣ������μ�NaOH��Һ��pH=4.0ʱ���õ�NaHX��Na2X�Ļ����Һ�����������ӵ�Ũ�ȴ���0.1mol/L��H2X��ҺԶС��0.01mol/L���ɴ˷������
��� �⣺A��ͼ��a��Ũ�ȴ���0.1mol/L������Na+��d��Ũ��С��0.01mol/L������H2X���ӣ���A��ȷ��
B�����ߵ����ǡ����ȫ��Ӧ����NaHX����Һ�����ԣ�˵��H2XΪ��Ԫ���ᣬHX-�ĵ���̶ȴ���ˮ��̶ȣ���B��ȷ��
C�����ݵ���غ�c��Na+��+c��H+��=c��HX-��+2c��X2-��+c��OH-���٣������غ��֪��c��Na+��=c��HX-��+c��X2-��+C��H2X���ڣ��ڴ���ٵã�c��H+��+C��H2X��=C��X2-��+c��OH-������C��ȷ��
D�����ݵ���غ�c��Na+��+c��H+��=c��HX-��+2c��X2-��+c��OH-���������μ�NaOH��Һ��pH=7.0ʱc��H+��=c��OH-��������c��Na+��=c��HX-��+2c��X2-������D����
��ѡD��
���� ���⿼�����������Һ�����жϣ��������ǿ����������غ㡢����غ������𣬿�������Ũ�ȴ�С�Ƚϡ���ҺPHֵ������ˮ��ȣ��ж�һԪ��HA������Ϊ����ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
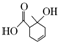
| A�� | �ܺ�̼������Һ��Ӧ�Ĺ�������2�� | |
| B�� | 1 mol���л����������2 mol H2�����ӳ� | |
| C�� | �� 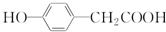 ��Ϊͬ���칹�� ��Ϊͬ���칹�� | |
| D�� | �ȿ��Է���ȡ����Ӧ�ֿ��Է���������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
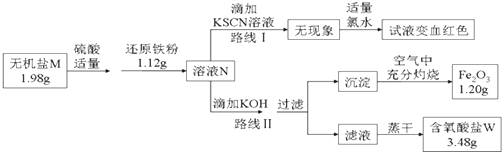
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �û���̿������װ��������к����� | |
| B�� | ��K2Cr2O7���˾���Ƿ�ƺ�ݳ� | |
| C�� | ��������ϴ�մ������ϵ����⼣ | |
| D�� | ��ʯ��ˮ����ȼú�����е�SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | �����������Ƿ�����ȥ��Ӧ | ��������NaOH�Ҵ���Һ���ȣ�������ͨ�뵽Br2��CC14��Һ�У��۲���Һ�Ƿ���ɫ |
| B | ��֤����H+������ HClO��HCO3- | ��NaHCO3��Һ�м���������ˮ���۲���Һ���Ƿ�������ð�� |
| C | ��֤H2O��NH3����λ����ǿ�� | ��CuSO4��Һ����μ������NH3•H2O���۲���ɫ��Һ�Ƿ�����ת��Ϊ����ɫ��Һ |
| D | ����Na2O2��ǿ������ | ��FeSO4��Һ�м�������Na2O2��ĩ���۲��Ƿ��к��ɫ�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ú��������ú��Һ����ú�ĸ�������ڻ�ѧ�仯 | |
| B�� | ���ۡ���ά�ء���֬�������ʾ����ڸ߷��ӻ����� | |
| C�� | ������ë�Ͳ�˿��������Ȼ�߷��� | |
| D�� | �մɡ�ˮ��Ͳ��������ڹ����β��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
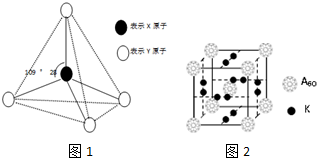
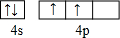 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com