
已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。
试回答下列有关的问题。
(1)写出F元素的电子排布式:_______________________________。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为_______________________________________。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是___。
(4)B、C、D、E的第一电离能由大到小的顺序是________(写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是________________________________(写化学式)。
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:
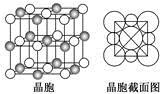
晶胞中距离一个B+最近的B+有________个。若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则E-的离子半径为________cm(含NA与ρ的式子表达)。
(1)1s22s22p63s23p63d54s1或[Ar]3d54s1
(2)sp3 (3)三角锥形
(4)Cl>P>S>Na NaOH>H3PO4>HClO4>H2SO4
(5)12 ,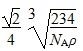
【解析】A、B、C、D、E、F六种元素,原子序数依次增大,由“A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等”及原子序数依次增大,推出A为O,由“B是短周期中原子半径最大的元素”推出B为Na,由“C元素3p能级层充满”推出C为P,由“F是第四周期未成对电子最多的元素”推出F为Cr,由“E是所在周期电负性最大的元素”及原子序数大小关系推出E为Cl,则D为S。(2)含四个原子的A的氢化物为H2O2,其氧原子的杂化轨道类型为sp3。(3)CE3和CE5为PCl3和PCl5,PCl3是极性分子,空间构型为三角锥形,PCl5为非极性分子。(4)同周期主族元素第一电离能从左到右有增大的趋势,但第ⅤA族反常,第一电离能由大到小的顺序是Cl>P>S>Na。四种元素最高价氧化物对应的水化物分别是NaOH、H3PO4、H2SO4、HClO4,NaOH是碱,H3PO4是中强酸,H2SO4、HClO4都是强酸,物质的量浓度相同时,pH由大到小顺序为NaOH>H3PO4>HClO4>H2SO4。(5)与Na+最近的Na+共有12个。设正方形(晶胞截面图)的边长为a cm、Cl-的半径为r cm,ρ a3=×58.5,得a=,r=a=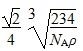 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014高考名师推荐化学--预测16 题型:填空题
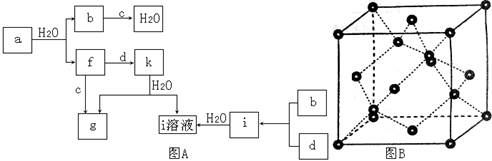
图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。
回答下列问题:
(1)图B对应的物质名称是 ,其晶胞中的原子数为 ,晶体的类型为 。
(2)d中元素的原子核外电子排布式为 。
(3)图A中由二种元素组成的物质中,沸点最高的是 ,原因是 ,该物质的分子构型为 ,中心原子的杂化轨道类型为 。
(4)图A中的双原子分子中,极性最大的分子是 。
(5)k的分子式为 ,中心原子的杂化轨道类型为 ,属于 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
向x mL 2.0 mol·L-1的盐酸中投入a g镁铝合金,金属完全溶解,再加入y mL 1.0 mol·L-1的NaOH溶液沉淀达到最大值,且质量为(a+1.7) g,则下列说法不正确的是
A.x=2y
B.镁铝合金与盐酸反应时转移电子的数目为0.1NA
C.镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12 L
D.a的取值范围为0.9 g<a<1.2 g
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:选择题
相对分子质量为100的有机物A能与钠反应,且完全燃烧只生成CO2和H2O。若A含一个六碳环,则环上一氯代物的数目为( )
A、5 B、4 C、3 D、2
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:选择题
下表所列各组物质中,不能通过一步反应实现如图所示转化的是
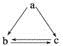
物质 选项 | a | b | c |
A | Si | Na2SiO3 | SiO2 |
B | Fe | FeCl3 | FeCl2 |
C | AlCl3 | Al(OH)3 | NaAlO2 |
D | Na2O2 | Na2CO3 | NaOH |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测13 题型:填空题
【物质结构与性质】
M是原子序数<30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于电子半充满状态。
(1)M原子的外围电子排布式为__________,在周期表中属于 区元素。
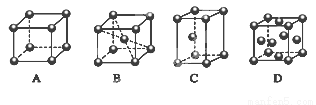
(2)M的堆积方式属于钾型,其晶胞示意图为______(填序号)。
(3)MCl3·6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3 B、[M(H2O)5Cl]Cl2·H2O和C、[M(H2O)4Cl2]Cl·2H2O。为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为 (填A或B或C)。
(4)MO2Cl2常温下为暗红色液体,熔点-96.5℃,沸点117℃,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①固态MO2Cl2属于________晶体;
②CS2中碳原子和丙酮(CH3COCH3)羰基中的碳原子分别采取的杂化方式为____杂化和________杂化。
(5)+3价M的配合物K[M(C2O4)2(H2O)2]中,配体是______,与C2O42-互为等电子体的分子是(填化学式)__________。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测13 题型:选择题
分子式为C5H10N2O3的二肽在酸性条件下可水解为氨基酸(不考虑H2N-COOH和立体异构),这些氨基酸重新组合可形成的二肽共有
A.3种 B.6种 C.9种 D.12种
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测12 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.7.8 g Na2O2中含有的离子总数目为0.4NA
B.1mol 苯分子中含有碳碳双键数目为3NA
C.标准状况下,将分子总数为NA的NH3和HCl气体混合后的体积约为22. 4L
D.16g CH4与18 g NH4+ 所含电子数均为10NA
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:选择题
下列有关说法正确的是
A.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解
C.反应N2(g)+3H2(g) 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大
2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大
D.吸热反应“TiO2(s)+2Cl2(g) TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0
TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com