
分析 (1)CeO2在稀硫酸和H2O2的作用下可生成Ce3+,Ce元素的化合价由+4价降低为+3价;
(2)从质量守恒、电荷守恒和电子守恒的角度配平方程式;
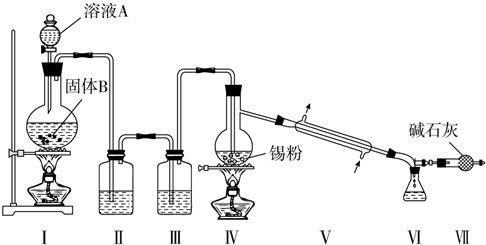
(3)由装置图可知装置Ⅰ应为制备氯气装置,涉及离子反应为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,装置Ⅱ为饱和食盐水,装置Ⅲ为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅳ中反应生成SnCl4,经冷却后在装置Ⅵ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅵ中,
①A为制备氯气装置,在加热条件下进行,应为浓盐酸和二氧化锰的反应;
②B为饱和食盐水,C为浓硫酸,氯气经除杂,干燥后与锡在D中反应生成SnCl4,因SnCl4极易水解,F可起到防止空气中的水蒸气进入E中;
③加热促进SnCl4气化,便于分离;
④用已知浓度的K2Cr2O7滴定生成的Fe2+,根据原子守恒、电子转移守恒可得关系式:Sn~Sn2+~2Fe3+~2Fe2+~$\frac{1}{3}$K2Cr2O7,据此计算.
解答 解:(1)CeO2在稀硫酸和H2O2的作用下可生成Ce3+,Ce元素的化合价由+4价降低为+3价,则CeO2在反应中作氧化剂,
故答案为:氧化;
(2)反应中Cr元素化合价由+6价降低到+3价,S元素化合价由+4价升高到+6价,则最小公倍数为12,由电子守恒和原子守恒、电荷守恒可知配平后的离子方程式为Cr2O72-+3SO32-+8H+═2Cr3++3SO42-+4H20,
故答案为:1;3;8H+;2;3;4;
(3)SnCl2在溶液中发生水解生成Sn(OH)Cl,其反应方程式为:SnCl2+H20?Sn(OH)Cl+HCl;
故答案为:SnCl2+H20?Sn(OH)Cl+HCl;
由装置图可知装置Ⅰ应为制备氯气装置,涉及离子反应为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,装置Ⅱ为饱和食盐水,装置Ⅲ为浓硫酸,氯气经除杂,干燥后与锡在装置Ⅳ中反应生成SnCl4,经冷却后在装置Ⅵ中收集,因SnCl4极易水解,应防止空气中的水蒸气进入装置Ⅵ中,
①装置Ⅰ中浓盐酸与MnO2在加热时发生反应产生氯气.发生反应的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
②由于盐酸有挥发性,所以在制取的氯气中含有杂质HCl,在与金属锡反应前要除去,因此装置Ⅱ中的最佳试剂为除去HCl同时还可以减少氯气消耗的饱和食盐水;SnCl4极易水解,在潮湿的空气中发烟.为了防止盐水解,所以要防止起水解.装置Ⅶ的作用为防止空气中的水蒸气进入Ⅵ中使SnCl4水解,
故答案为:饱和氯化钠溶液;防止空气中水蒸气进入Ⅵ中,SnCl4水解;
③如果没有装置Ⅲ,则在氯气中含有水蒸汽,所以在Ⅳ中除生成SnCl4外,还会生成SnCl4水解产生的含锡的化合物Sn(OH)4或SnO2,加热促进SnCl4气化,便于分离,
故答案为:加热促进SnCl4气化,便于分离;
④令锡粉中锡的质量分数为x,则:
Sn~Sn2+~2Fe3+~2Fe2+~$\frac{1}{3}$K2Cr2O7
M g $\frac{1}{3}$mol
mx g cV mol
故 M g:mx g=$\frac{1}{3}$mol:cV mol
解得x=$\frac{3cVM}{M}$,
故答案为:$\frac{3cVM}{M}$.
点评 本题考查物质的制备,涉及仪器的识别、氯气的实验室制取方法、实验操作的目的、盐的水解、物质产率的计算等知识,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力的考查,注意把握题给信息,结合物质的性质设计实验步骤,题目难度不大.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| Y | V | |||
| X | W |
| A. | 原子半径:X>W>V>Y | |
| B. | Y的最高价氧化物的电子式为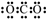 | |
| C. | X的最高价氧化物能与V、W最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时所生成的物质为离子化合物,既含有离子键又含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某气体通入FeCl2溶液中 | 溶液由浅绿色变为黄色 | 该气体中一定含有Cl2 |
| B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体中一定含有SO2 |
| C | 将某气体通过灼热的CuO粉末 | 粉末由黑变红 | 该气体中一定含有H2 |
| D | 将某气体与湿润的红色石蕊试纸接触 | 试纸变蓝色 | 该气体中一定含有NH3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇 | B. | 甲酸 | C. | 甲醛 | D. | 甲酸甲酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C15H31COOH和C17H35COOH是同系物 | |
| B. | 结构不同,性质相同,化学式相同的物质互称同分异构体 | |
| C. | 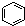 和 和 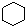 均是芳香烃, 均是芳香烃,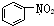 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 | |
| D. | 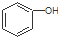 和 和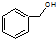 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1 mol KClO3参加反应,有2 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 压缩容器体积,增大压强,活化分子百分数不变,化学反应速率增大 | |
| B. | 升高温度,活化分子百分数增大,化学反应速率增大 | |
| C. | 加入反应物,活化分子百分数增大,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应所需的活化能,活化分子百分数增大,化学反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应原理 | 实验装置 | 实验步骤 |
(1)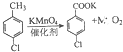 (2) 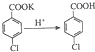 | 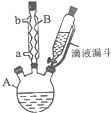 | ①在规格为250mL的仪器A中加入一定量的催化剂(易溶于有机溶剂)、适量KMnO4、100mL水; ②安装好仪器,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯; ③控制温度在93℃左右,反应2h,趁热过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩,冷却; ④再次过滤,将滤渣用冷水进行洗涤,干燥后称得其质量为7.19g |
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 属于可溶性盐 | |||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com