
 计算物质的量,结合质量数=质子数+中子数计算分析判断;
计算物质的量,结合质量数=质子数+中子数计算分析判断; 计算溶质和溶剂物质的量,结合乙醇和水分子式计算氢原子数.
计算溶质和溶剂物质的量,结合乙醇和水分子式计算氢原子数.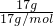 =1mol,所含中子数=1mol×(14-6+0)×NA=8NA,故A错误;
=1mol,所含中子数=1mol×(14-6+0)×NA=8NA,故A错误;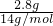 ×1×NA=0.2NA,故C错误;
×1×NA=0.2NA,故C错误;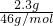 =0.05mol,水物质的量=
=0.05mol,水物质的量=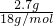 =0.15mol,氢原子的总数=(0.05mol×6+0.15mol×2)×NA=0.6NA,故D正确;
=0.15mol,氢原子的总数=(0.05mol×6+0.15mol×2)×NA=0.6NA,故D正确;

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com