
| A、氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH)3↓ |
| B、氯化铝溶液通入过量氨水:Al3++4OH-→AlO2-+2H2O |
| C、碳酸氢钠溶液与盐酸:HCO3-+H+=H2O+CO2↑ |
| D、钠投入水中:2Na+2H+→2Na++H2↑ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
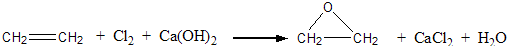
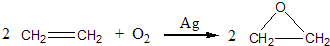
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
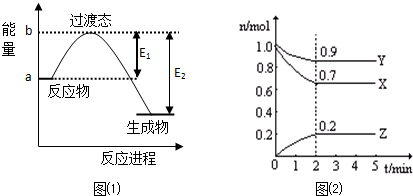
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol.L-1 KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、0.1mol.L-1 NaOH溶液:Na+、Ca2+、I-、NH4+ |
| C、中性溶液:Fe3+、Al3+、NO3-、SO42- |
| D、c(H+)水电离=10-12 mol?L-1的溶液:Ba2+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠着火燃烧时,用泡沫灭火器灭火 |
| B、含硫酸的废液倒入水槽,用大量水冲入下水道 |
| C、氢氧化钠应该保存在带有橡胶塞的试剂瓶中 |
| D、稀释浓硫酸时,要慢慢地把适量水加进去,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol?L-1甲酸溶液的pH值约为2 |
| B、甲酸电离出的阳离子全部是H+ |
| C、10mL 1mol?L-1甲酸与10mL 1mol?L-1 NaOH溶液完全反应后,溶液呈碱性 |
| D、1L H+浓度为0.1mol?L-1的甲酸和足量Zn反应放出的H2在标况下远大于1.12L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com