
【题目】资料一:考古工作者从安阳的商代铸铜遗址中,发现当时冶炼铜的主要矿物原料是孔雀石(Cu2(OH)2CO3),主要燃料是木炭,冶炼温度估计在1000℃左右.
资料二:西汉刘安著《淮南万毕术》中记载“曾青得铁则化为铜”.“曾青”可能是硫酸铜一类的物质,将孔雀石溶于硫酸中得此溶液,当把铁粉投入此溶液中即可得铜.
(1)关于“曾青”和孔雀石的水溶性分析中,判断正确的是__________
A.前者可溶,后者难溶 B.前者难溶,后者可溶
C.两者均可溶 D.两者均难溶
(2)以孔雀石为原料的冶炼过程中,用现代化学的观念审视,可能涉及的化学反应有__________
①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
②2CuO+C ![]() 2Cu+CO2↑
2Cu+CO2↑
③CuO+CO ![]() Cu+CO2
Cu+CO2
④CO2+C ![]() 2CO
2CO
A.①② B.①③ C.①②③ D.①②③
(3)在(2)的四个反应中,不属于四种基本反应类型的有(填序号,下同)__________,不属于氧化还原反应的有__________.
(4)资料二中,假设溶解孔雀石的酸是稀硫酸,写出用此方法冶炼铜的化学方程式 ______________________________________________,
【答案】 A D ③ ① Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O、 CuSO4+Fe=FeSO4+Cu.
【解析】试题分析:(1)由资料一:孔雀石为矿物原料,可知孔雀石难溶于水,由资料二:“曾青得铁则化为铜”可知铁把铜从它的盐溶液中置换出来,所以“曾青”可溶于水,答案选A。
(2)孔雀石为原料的冶炼时可能涉及的反应为,孔雀石高温分解生成氧化铜、水和二氧化碳;碳还原氧化铜生成铜和二氧化碳;碳和二氧化碳生成一氧化碳;一氧化碳具有还原性还原氧化铜,答案选D。
(3)反应①为一种物质生成三种物质,属于分解反应;反应②④均为单质和化合物生成另一种单质和化合物,属于置换反应;反应③不符合四种基本反应类型;①没有化合价的变化,其它均有化合价的变化,答案选①。
(4)孔雀石的主要成分是碱式碳酸铜,可与稀硫酸反应生成硫酸铜、水和二氧化碳,化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O;然后用铁还原硫酸铜,化学方程式为CuSO4+Fe=FeSO4+Cu。


科目:高中化学 来源: 题型:
【题目】下列物质在应用中,只应用其化学性质的是
A. 将活性炭放入冰箱中除去异味B. 用铅笔芯粉末使锁的开启变的更灵活
C. 用二氧化碳灭火D. 用一氧化碳来冶炼生铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下CO2、H2、CO的混合气体与氮气的密度相同,则该混合气体中CO2、H2、CO的质量之比可能为( )
A.13:8:27
B.13:9:27
C.26:16:27
D.286:8:27
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 原电池中的电极一定要由两种不同的金属组成
B. 原电池两极均发生氧化还原反应
C. 原电池中电子流出的一极是正极,发生氧化反应
D. 原电池中阳离子向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( ) 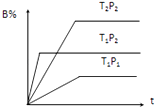
A.T1<T2、P1>P2、m+n>p,△H<0
B.T1>T2、P1<P2、m+n>p,△H>0
C.T1>T2、P1<P2、m+n<p,△H>0
D.T1<T2、P1>P2、m+n<p,△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应 2Y2Z2 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( ) 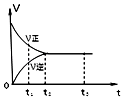
A.t1时,只有正方向反应
B.t2﹣t3 , 反应不再发生
C.t2﹣t3 , 各物质的浓度均没有发生变化
D.t2时,反应到达限度,正反应和逆反应速率相等且等于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( ) 
A.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应
B.图一所示当有0.1mol电子转移时,有0.1mol Cu2O生成
C.图二装置中发生:Cu+2Fe3+═Cu2++2Fe2+ , X极是负极,Y极材料可以是铜
D.如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2═NF3+3NH4F.在潮湿的空气中,NF3能与水蒸气发生氧化还原反应,其反应的产物有HF、NO和HNO3 . 下列说法正确的是( )
A.制取NF3的反应中,氧化剂与还原剂的物质的量之比为3:1
B.在NF3与H2O的反应中,H2O作还原剂
C.若在制取NF3的反应中有0.5 mol NH3参加反应,转移电子的物质的量为3 mol
D.NF3在空气中一旦泄漏,不易于发现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验。
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气________(填“漏气”、“不漏气” 或“无法确定”)
(2)写出C装置中反应的化学方程式:_________
(3)若装置是不漏气的,打开止水夹a后,用上述装置进行实验。写出A中发生反应的化学方程式,并用双线桥标出化合价变化情况、电子转移的方向和数目及被氧化还原情况 _________
(4)B装置中盛放的试剂是__________,其作用是___________ D仪器名称是 _____
(5)Fe(OH)2 在潮湿空气中变成灰绿色、红褐色:_________

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com